Kemoterápia által kiváltott hányinger és hányás
Karen M. Mustian
1 Rochester-i Egyetem Orvosi és Fogorvosi Egyetem, James P. Wilmot Rákközpont, Box 704, 601 Elmwood Avenue, Rochester, NY 14642
A kezelés előrehaladtával szemben a hányinger és a hányás, különösen a megelőző hányinger és a hányás, az émelygés és a hányás késleltetése, valamint a hányinger továbbra is a leggyakoribb, várható és félelmet káros mellékhatások a kemoterápiában részesülő betegek körében. A rákos betegek 70-80% -a, akiknél a kemoterápia által kiváltott hányinger és hányás tapasztalható, késlelteti vagy megtagadja a jövőbeli kemoterápiás kezeléseket, és a további hányingertől és hányástól való félelem miatt minden kezelést leáll. Ennek a fejezetnek az a célja, hogy áttekintést nyújtson a CINV pato-pszichofiziológiájáról, a szokásos kezelés ajánlott irányelveiről, és kiemelje az újabb célzott kezelési megközelítéseket.
Bevezetés
A rákkezelést és mellékhatásukat sok betegnek gyakran gyengítik, mint a tényleges rák. Az émelygés és a hányás (NV) a kemoterápiában részesülő betegek között a leggyakoribb, várható és félelmet keltő mellékhatások közé tartozik. Valójában egyes rákos betegek, akik kemoterápia által kiváltott hányinger és hányás (CINV) tapasztaltak, késleltetik a kemoterápiás kezeléseket, és meggondolják, hogy a későbbi kezelések megtagadják a további NV félelem miatt. 1-4 Előzetes hányinger és hányás (ANV) szintén problémák jelentkeznek a kemoterápiás betegek között. A negyedik kezelési ciklusban előzetesen hányingerről számoltak be olyan betegek legfeljebb 30% -ánál, akik hányingerben részesültek a korábbi kemoterápiás ciklusok után, 5 míg az előzetesen hányás mértékét 20% -ig jelentették. A CINV alacsonyabb kemoterápiás tapadáshoz vezet, csökkent funkcionális aktivitást, megnövekedett szorongást és depressziót, csökkent életminőséget (QOL), valamint az egészségügyi forrás erőteljesebb kihasználását eredményezi, ami jelentősen növeli a rák terheit és hatékony kezelését. 4, 8-11 Nagyon nagy előrelépés történt az akut CINV hatékony kezelésében, bár a késleltetett CINV és a hányinger önmagában is jelentős problémák. 1, 2 A fejezet célja, hogy áttekintést nyújtson a CINV patopszichofiziológiájáról, a szokásos kezelés ajánlott irányelveiről, és kiemelje az újabb célzott kezelési módszereket.
Az émelygés és a hányinger kórtörténetében
Émelygés és hányinger pathopsihológiája
Kondicionáló és Előzetes Hányinger és Hányás
Az ANV szerencsétlen következménye a CINV-nek, amelyet a kezelés előtt a hányinger és / vagy a hányás előfordulása jellemez. A többség, ha nem minden, a kutatók egyetértenek abban, hogy az ANV kialakulása szorosan összefügg a Pavlov kondicionáló modellel (lásd az 1. ábrát), ahol a betegek még mindig képesek ANV-t tapasztalni anélkül, hogy az utókezelést megelőző NV-t. 12 ANV a negyedik kezelési ciklusban a korábbi kemoterápiás ciklusokat követő hányingert és / vagy hányást okozó betegek körülbelül 30% -ában fejlődik ki. 5 ANV kezdődik, amíg a páciens még otthon vagy a rák klinikán jár. Az ANV gyakran fokozatosan növekszik, amikor a beteg közeledik a tényleges teremhez, ahol kezelésben részesülnek. Az ANV olyan probléma, amely hátrányosan befolyásolja a betegeket a QOL 7, 13 betegeknél, és egyes esetekben zavarhatja a beteg kezelésének megszakításáig. 14 Ha az ANV kialakul, akkor nem szabályozható normál antiemetikus gyógyszerekkel, beleértve az 5-HT-t3 receptor antagonisták. 15
Émelygés és hányás klasszikus kondicionálása
Várakozás és émelygés
A placebo és / vagy nocebo hatások hozzájárulhatnak az antiemetikák hatástalanságához az ANV kezelésében, különösen az émelygésben. A Kirsch 16 azt sugallja, hogy egy élettani szenzációra, például émelygésre vonatkozó várakozás vagy válaszadási reakció megfelelő szubjektív élményeket generálhat, és amennyiben ilyenek, önmagát erősítik. Ha ilyen várakozások természeténél fogva nem kívánatosak (például émelygés a káros ingerektől), Kirsch elméjti, hogy a várakozások közvetlenül befolyásolják mind a fiziológiai, mind a pszichológiai kimeneteleket, önmagukat megerősítik és a placebo-hatásra utalnak. Stewart-Williams azt állítja, hogy a várakozások a legtöbb placebo-hatás legfontosabb elemei az emberekben. 17 A Forgione 18 azt sugallja, hogy “a placebót úgy lehet gondolni, mint véletlenszerű várandósságot.” Hahn 19, valamint Barsky és munkatársai 20 azt javasolja, hogy a mellékhatások (pl. Émelygés) kialakulásának elvárásai mellékhatásokat okozhatnak a nocebo . A klinikai környezetben a várható élettartamot és a placebót vizsgáló 93 vizsgálat áttekintése arra a következtetésre jutott, hogy a várakozások központi szerepet játszanak az orvosi mellékhatások kialakulásában, és az a fő mechanizmus, amellyel a placebos élettani hatásokat vált ki. 21
A klasszikus kondicionáló paradigma nem teljesen magyarázza meg az ANV kialakulását, a 22, 23-at és a kognitív tényezők, például a szorongás és a válaszadási várakozások szerepe az ANV fejlődésében. 7, 24-26 A szorongásról ismert, hogy befolyásolja az NV fejlődését legalább részben a negatív várakozásokon keresztül, 24, 27-29, és kölcsönösen negatív várakozások játszanak szerepet a szorongás kialakulásában. 16, 30 A kilátások befolyásolják a kondicionáló hatások kialakulását, 31-33 és fordítva, a kondicionáló hatás befolyásolja a várakozásokra adott válaszokat. 16, 34, 35 Ezért a szorongás és a válaszadási várakozások közvetíthetik a páciensek kondicionálását az ANV felé. Számos tanulmány kimutatta, hogy a válaszadási várakozások jelentősen megjósolják az ANV 23, 26, 36-38 előfordulását A kutatócsoportunk által lefolytatott, 63 különböző típusú rákos női rákos betegek által leíró leíró vizsgálat azt mutatta, hogy a várható élettartam erőteljesen megjósolta az émelygés kialakulását a harmadik kemoterápia (p = 0,001). Az émelygés várakozását az első kezelést megelőzően egy ötpontos szemantikus besorolási skála alapján értékelték, melynek egyik végén “1” = “Biztos vagyok benne, hogy nem lesz hányinger”, a másik pedig “5” = ” Biztos vagyok benne, hogy hányingerkorzom. “36 (Lásd a 2. ábrát)
A páciensek aránya a megelőző hányingerről a 3. ciklus előtt a hányingerre vonatkozó bizonyosság előkezelésének mértéke.
A CINV gyakoriságának és súlyosságának változását a betegek kemoterápiás szerek farmakológiai tulajdonságai vagy fiziológiai jellemzői nem tükrözik teljes mértékben. 39, 40 A betegek elvárásai a CINV kifejlesztésére vállalták, hogy ennek a varianciának egy részét számolják el, és számos tanulmány pozitív kapcsolatot mutatott a betegek CINV fejlesztési elvárásai között. Például, Roscoe és kollégái 44 194 emlőrákos beteget tanulmányoztak, akik megkezdték a doxorubicint tartalmazó első rákkezelési rendet (lásd a 2. ábrát). Az eredmények azt mutatták, hogy az első kemoterápiás ciklus megkezdése előtt értékelt hányinger várható betegei a későbbi émelygés erős előrejelzői voltak, és a súlyos hányinger erősebb prediktora volt, mint a korábban bejelentett tényezők, mint például az életkor, a terhesség alatt fellépő hányinger és a mozgásérzékenység betegség. Azok a betegek, akik úgy vélték, hogy “nagyon valószínű”, hogy kemoterápiát követően súlyos hányingerben szenvednek, ötször nagyobb valószínűséggel tapasztaltak súlyos hányingert azokkal szemben, akik azt jelezték, hogy “nagyon valószínűtlen” lenne, hogy a kemoterápia után súlyos hányingert tapasztalnak. Ezek az eredmények arra engednek következtetni, hogy a betegek várható hányingerei a CINV-nek, különösen az émelygésnek, jelentős előrejelzői és valószínűleg hozzájárulnak a CINV-hez.
Émelygés és hányás patofiziológiája
A hányás patofiziológiája sokkal egyenletesebb, és úgy gondolják, hogy az agyi cortex és más, magasabb fejlettségű területek általános bevonása nélküli alsóbb agyi struktúrákra terjed ki. 45 A hányás mérgező anyagok, például kemoterápiás szerek által kiváltott reflex. Általánosságban ezek a szerek a gyomor- vagy kismedencei nyálkahártyában észlelhetők, és a központi idegrendszerrel (CNS) kölcsönhatásba lépő vagális afferensek stimulálják, ami efferens vagális hatáshoz vezet, ami végül hányingerhez vezet. 8, 46 A hányinger és / vagy hányinger időbeli előfordulása, súlyossága és mértéke változó, és nagymértékben befolyásolja a nem, a faj és az életkor, valamint az aktuális és a múltbeli egészségi állapot. 47. A hányásváltozás biológiai tulajdonságainak jelenlegi ismerete és arról, hogy az egyének miként válaszolnak másképp a kemoterápiára, az NV kezelésére szolgáló terápiás kezelések fejlesztésében segített. A kemoterápia által kiváltott hányás megelőzésében és ellenőrzésében elért haladás a kemoterápiában a kemoterápiában bekövetkező hányást észlelte, míg az emetogén kemoterápiát kapó betegek többségénél a kezelés folyamán még mindig jelentkeznek hányinger. 48
A vegyület / receptor jelátvitel kulcsfontosságú a hányinger megválaszolásához és szabályozásához. A legszélesebb körben vizsgált vegyület a szerotonin, más néven az 5-HT. Az 5-HT-t enterochromaffin sejtek termelik, amely egyedülálló típusú sejtek diszpergálódnak az enterális hámban. Ezek a sejtek konstitutívan expresszálják az 5-HT-t és egy kemoterápiás ágensnek való expozíció után az 5-HT-t bőségesen fejezik ki. Magasabb szinten az 5-HT felszabadul a bazális felületről a lamina propria-be. Ott, a szekretált 5-HT kötődik az 5-HT rokonaihoz3 receptorokat, amelyek a vagus idegterminálokon helyezkednek el, így neurotranszmitterként működnek, amely jelet továbbít a hátsó végtagnak. A fordított jel viszont egy NV motorválaszát váltja ki, melyet a vagális idegek efferentálnak. Annak érdekében, hogy az 5-HT-vel közvetített NV-válasz endogén véget érjen, a vegyületet a SERT receptor kötődésével bél enterocitákkal kell felvenni. 50
Körülbelül 20 éve, az 5-HT3 antagonisták rendkívül hasznosak a kemoterápiában részesülő betegek NV csökkentésére. Ezek a gyógyszerek az 5-HT-hez kötődő 5-HT-vel versenyeznek hányásellenes hatásukkal3 receptorokat, ezáltal megakadályozva a központi idegrendszeri pro-etiiás jelet. A legújabb 5HT3 antagonista, a palonosetron, magasabb receptor-kötő affinitással rendelkezik, mint a többi szokásos 5HT3 antagonisták, amelyek hatásosabbá tehetik az NV megakadályozását. Ezenkívül a hatóanyag felezési ideje 40 óra, ami lehetővé teszi a késleltetett NV hatékonyabb megelőzését, mint amit más 5-HT-vel3 antagonoists. 51 Mivel az 5-HT szintézis szignifikánsan megemelkedik a kemoterápia után, egy másik lehetséges terápiás előnyös módszer csökkenti az 5-HT szintézist a bélben. Mivel a HT szintézise a triptofán-hidroxiláz (TPH) függvénye, ez az enzim életképes célpontot jelenthet. Valójában a pre-klinikai vizsgálatok egy TPH-inhibitort alkalmaztak az 5-HT szelektív gátlására a bélben egy kemoterápiával indukált hányás görényes modelljével. 52
A P anyag egy másik erős szabályozó a hányingerre; kötődik a neurokinin-1 receptorhoz (NK-1). Mind a vegyület, mind a receptor megtalálható a központi idegrendszerben és a bélben is. Az 5-HT / 5HT-től eltérően3 receptor-interakció, kevésbé ismert arról, hogyan és hol a P anyag és a neurokinin-1 a hányáspotenciál elősegítésében járnak el, bár perifériás és központi komponensek is szerepet játszhatnak. A preklinikai vizsgálatok azt mutatják, hogy a központi idegrendszeri neurokinin-1 receptor antagonizáló hatása kulcsfontosságú az NV megakadályozásában, mivel a vér-agy gáton át nem képes anyagok nem védik a hányást. Klinikailag az aprepitantnak az első, az NK-1 receptor antagonizálására kifejlesztett gyógyszerkészítmény bizonyult hatásosnak az NV megelõzésében, amikor az alkalmazott terápiákkal kombinálják. 54
A dopamin-felszabadulás és a rokon vegyület dopamin receptor-2 jelátvitele szintén szerepet játszhat, mivel a dopamin-antagonisták hatásosnak bizonyultak az NV kezelésében, bár sokkal kevésbé ismert ez a mechanizmus. Végül, míg a központi idegrendszer részvétele nyilvánvalóan jelentős szerepet játszik a hüvelyi folyamatban, lehetséges, hogy az ENS (bélben oldódó idegrendszer) maga is képes szabályozni az NV-hatásokat a CNS interplay nélkül. A kevésbé megértett mediátorok szerepének további megértése hozzájárulhat az antibiotikum kezelésének szélesebb köréhez az NV teljes körű megelőzéséhez és különböző NV-es betegek kezelésében.
Jelenlegi tudományos bizonyítékok a kemoterápia által kiváltott hányinger és hányás kezelésére vonatkozóan
viselkedési
Egy növekvő irodalmi háttér támogatja a viselkedési beavatkozások hatékonyságát a CINV, különösen az ANV kezelésére. A viselkedési beavatkozások különösen alkalmasak az ANV kezelésére, mivel kondicionált válasz 55, 56 és ezek a legjellemzőbbek a nemkívánatos kondicionált válasz teljes / teljes kifejlődése előtt. Sok olyan beavatkozás, amely hatékonyan befolyásolja az NV-t, sikeresen alkalmazták az ANV számára. 57, 58 Egy olyan beavatkozás, amely késleltheti vagy megelőzheti a kezelés kondicionált mellékhatásait 59, az progresszív izomlazítás (PMR), amely során progresszív módon megfeszítik az izomcsoportok tenyésztését és felszabadulását. 56 A PMR-t szedő betegek szignifikánsan kevesebb hányingerről számoltak be a kemoterápia 60 alatt és közvetlenül, és NV csökkent időtartamúak voltak. A PMR-nek jelentős hatása van az émelygés szabályozásában. 62 A pihenés gyakran irányított képekkel kombinálva (a figyelem középpontjába a specifikus élettani válaszok kiváltására és konkrét egészségügyi célok elérésére irányulnak). Az imázs mentálisan foglalkozik az összes érzékszervi modalitással, így mind a pszichológiai, mind a fiziológiai válaszok generálódnak, mintha tényleges külső inger jelenne meg. 63 A csendes jeleneteket ábrázoló irányított képek 55 és a pácienspecifikus és az értelmes képek körül kialakított képek, amelyeknek mellékhatásai vagy betegségei kedvezőek. 58, 64 A relaxáció és a vezetett képalkotás kombinált beavatkozásával járó betegek csökkent kemoterápiás előfordulási gyakorisággal, a kemoterápia utáni hányinger alacsonyabb incidenciájával, időtartamával és súlyosságával, a kezelés utáni hányás rövidebb időtartamával, 65, 66 és újabb pozitív tapasztalat a kemoterápiában, mint azok, akik kizárólag antiemetikus kezelést kapnak. 67 Egyéb beavatkozások közé tartozik a hipnózis, vagy a szuggeszti terápia 68-71 szisztematikus deszenzitizáció 72 biofeedback, 56 csuklópánt, 73 és elektromos stimuláció a csuklón. 74
Ezeknek a viselkedési beavatkozásoknak egyetlen szállítási módja sem általános, sem hibátlan. Ezeknek a stratégiáknak az egy-egy utasítása (klinikum a páciens számára) lehetővé teszi a klinikus számára, hogy személyre szabja az egyéni páciens preferenciáit, és hatékonyabb, mint az audiokazettákkal való oktatás, 75 azonban az audiotapes lehetővé teszi az élő beavatkozás utáni független gyakorlatot 59 és költséghatékony . 56 A beavatkozások végrehajtásának megválasztásakor figyelembe kell venni a beteg szükségleteit, erőforrásait, képességeit, pszichológiai előzményeit és állapotát, valamint a kezelés helyét. 64
Gyógyszeripari
Az első generációs antiemetikus szerek előrehaladása és az új terápiák bevezetése elősegítette a CINV kontrollját; a palonosetron (Aloxi) és az aprepitant (Emend) a két legújabb antiemetikum. Palonosetron, egy második generációs 5-hidroxi-triptamin-3 (5-HT3) receptor antagonista, erős antiemetikus szer, nagyobb kötési affinitással (100-szor nagyobb) a 3. típusú szerotonin receptorhoz és hosszabb felezési idővel (
40 óra, 5x hosszabb), mint az osztályban lévő egyéb gyógyszerek. 8, 10, 11, 76 Egyszeri dózis (0,25 mg IV) a palonoszetron hatásos akut és késleltetett NV-k hatékony megelőzésére közepesen magas emetogén kemoterápiához és ugyanolyan hatásos, mint az idősebb antiemetikus szerek. 8, 10, 11, 76 Egyes tanulmányok kimutatták, hogy a palonosetron jobb, mint az első generációs 5-HT3 receptor antagonisták (ondansetron és dolasetron), de csak a másodlagos végpontoknál (a késleltetett hányás megelőzése és az általános tolerálhatóság), mivel az elsődleges végpontok teljesültek (hányás és nem mentő gyógyszerek szükségesek) minden vizsgálatban. 8, 76, 77 A legfontosabb kérdés nem a palonosetron lehetséges magasabb rendű felesége a régebbi 5-HT-nek3 receptor antagonistákat, hanem inkább azt, hogy a palonosetron jobb-e a korábbi 5-HT-nél3 receptor antagonistákkal kombinálva más gyógyszerekkel (különösen dexametazon, kortikoszteroid és aprepitant) kombinálva. 76 Nem történtek prospektív vizsgálatok, amelyek kifejezetten a palonosetron felett álló képességének bizonyítására szolgáltak az 5-HT felett3 receptor antagonista és nincs prospektív kísérlet, amely összehasonlította a palonosetront egy másik 5-HT-vel3 receptor antagonista, amikor mindkettőt kombinálják a dexametazonnal. 8 A jövőbeni tanulmányoknak meg kell vizsgálniuk az antiemetikus szerek különböző kombinációinak (régebbi és újabb szerek kombinációinak) hatását, és meg kell határozniuk a CINV megelőzésére és szabályozására szolgáló optimális kombinációt.
Aprepitant, egy neurokinin-1 (NK1) receptor antagonista, az antiemetikumok legújabb osztályát képviselik. A III. Fázisú vizsgálatok kimutatták, hogy az aprepitant hatékonyan befolyásolja a CINV-t. Számos összehasonlító vizsgálatban a többszörös kezelési ciklusokon keresztül a tartós antiemetikus védelem az aprepitant csoportban jobb volt, mint a kontroll csoportban. 8, 78-81 A jelenlegi iránymutatások szerint 82-84 egy 3-kábítószer-kombináció egy 5-HT3 a magas emetikus kockázatú kemoterápia előtt ajánlott a szerotonin receptor antagonista, a dexametazon és az aprepitant alkalmazása; egy 5-HT-et tartalmazó három gyógyszeres kombináció3 szerotoninreceptor-antagonista, dexametazon és aprepitant vagy az 5-HT kétszeres kombinációja3 szerotonin receptor antagonista és dexametazon a mérsékelt emetikus kockázat miatt (a kemoterápiás rendszertől függően); és a dexametazon csak alacsony emetikus kockázat esetén.
Az új antiemetikus terápiák bevezetése ellenére az első generációs antiemetikus szerek továbbra is a CINV kezelésére szolgálnak. Két régebbi 5-HT3 receptor antagonisták (ondansetron és granisetron), amelyek továbbra is hatékony antiemetikus lefedettséget biztosítanak a CINV számára, lehetnek olcsóbbak, mint az újabb hatóanyagok, és nagyobb valószínűséggel fedezhetők a beteg egészségbiztosítása. 85 Számos tanulmány kimutatta, hogy az ondansetron és a granisetron mind a CINV primer (teljes kontroll vagy hányás), mind másodlagos (megelőző késleltetett hányás) megelőzésére hatásos. Emellett a mellékhatások (fejfájás, csuklás, hasmenés, székrekedés, álmosság, túlérzékenység, remegés) mindkét gyógyszer enyhe és rövid időtartamú. Mindazonáltal, az idősebb antiemetikus szerek és az újak ígéretének folyamatos hatékonysága ellenére a CINV a rákos megbetegedések fő problémájaként továbbra is fennáll. Míg az elsődleges probléma a hányás megelőzése, az émelygés problémája nagyobb kihívássá válik, mivel a hányásszabályozás stratégiái javulnak. 1
Kezeléssel összefüggő hányinger és hányás (PDQ®) -Health Professional verzió
Az émelygés és a hányás megelőzése és ellenőrzése (hányás) (NV) a rákos betegek kezelésében kiemelt fontosságú. A kemoterápiával indukált NV az egyik leginkább fájdalmas akut mellékhatás a rákkezelésben; a betegek legfeljebb 80% -ában fordul elő, és jelentős hatással lehet a páciens életminőségére. NV az alábbiakat is eredményezheti:
- Súlyos anyagcserezavarok.
- Táplálékkifejtés és anorexia.
- A páciens fizikai és szellemi állapotának romlása.
- Nyelőcső könnyek.
- Törés.
- Sebszétválás.
- A potenciálisan hasznos és gyógyító daganatellenes kezeléstől való kilépés.
- Az öngondoskodás és a funkcionális képesség degenerációja.
Ebben az összefoglalóban, hacsak másként nem jelezzük, a felnőttekhez kapcsolódó bizonyítékokat és gyakorlatokat kérdeznek meg. A gyermekekkel kapcsolatos bizonyítékok és gyakorlati alkalmazások jelentősen eltérhetnek a felnőttekkel kapcsolatos információktól. Amikor rendelkezésre állnak a gyermekek gondozásával kapcsolatos konkrét információk, a saját címsorában foglalják össze.
Kórélettani
A hányinger szubjektív jelenség a kellemetlen, hullámos érzésnek a torokban és / vagy az epigastriumban, amely hányás (hányás) csúcspontja. A hányás a szájüregen keresztül a gyomor, a nyombél, vagy a jejunum tartalmának kitolódása. A retching a hányás gyomor és nyelőcső mozgását vonja maga után a hányás kizárása nélkül; Szárazságnak is nevezik.
Előrelépés történt az émelygés és a hányás (NV) irányítását befolyásoló neurofiziológiai mechanizmusok megértésében. Mindkettőt a központi idegrendszer szabályozza vagy közvetíti, de különböző mechanizmusok. Az émelygést az autonóm idegrendszer közvetíti. Hányás egy komplex reflex stimulálásával, amely az afferens stimuláció konvergenciáját tartalmazza a következőkből: [1,2]
- Kemooreceptor-indítózóna (CTZ, terület postrem).
- Az agykéreg és a limbikus rendszer érzékeny stimulációra adott válaszként (különösen szag és íz), pszichológiai szorongás és fájdalom.
- A belső fül vestibularis-labirintus berendezései a testmozgásra válaszul.
- A zsigeri szervek és a vaszkuláris perifériás ingerek (vagális és spinalis szimpatikus idegek révén) exogén vegyi anyagok és endogén anyagok hatására, amelyek gyulladás, ischaemia és irritáció során felhalmozódnak.
A neurotranszmitterek (köztük a szerotonin, a P anyag és a dopamin található a CTZ-ben), a hányásközpont (a sejtmagban található a nucleus tractus solitariusban) és az enterochromaffin sejtek a gasztrointesztinális traktusban, majd effervens impulzusokat bocsátanak ki, salivációs központ és légzőközpont. Az NV szimptómáktól csúcsosodó többszörös útvonalak viszonylagos hozzájárulása komplex, és feltételezhető, hogy figyelembe veszi a változó emetogenitást (belső emetogenitás és enyhítő tényezők [azaz dózis, beadási útvonal és expozíció időtartam]) és emetogén profil (vagyis a kezdeti időpont , a tünetek súlyossága és időtartama) [3,4]
Irodalom
- Wickham R: A kemoterápia által kiváltott hányinger és hányás kezelési paradigmái. Cancer Control 19 (2 Suppl): 3-9, 2012. [PUBMED Abstract]
- Navari RM: Antiemetikus kontroll: az emetogén kemoterápia új gondozásának színvonala felé. Expert Opin Pharmacother 10 (4): 629-44, 2009. [PUBMED Abstract]
- Cefalo MG, Ruggiero A, Maurizi P, et al .: A kemoterápia által kiváltott hányinger és hányás farmakológiai kezelése rákos gyermekekben. J Chemother 21 (6): 605-10, 2009. [PUBMED Abstract]
- Darmani NA, Crim JL, Janoyan JJ és munkatársai: A kemoterápia által indukált azonnali és késleltetett hányás neurotranszmitter alapjainak újraértékelése: a legkevésbé bizonyított bizonyíték. Brain Res 1248: 40-58, 2009. [PUBMED Abstract]
Általános kockázati tényezők és etiológiák
Bár a kemoterápiában részesülő betegek többsége hányinger és hányás (hányás) kockázatának van kitéve, a kezdetektől, súlyosságtól, kiváltó tényezőktől és az időtartamtól függ. A tumorral, a kezeléssel és a beteggel kapcsolatos tényezők mind hozzájárulnak az NV-hez, beleértve a tumor elhelyezkedését, a kemoterápiás szereket és a sugárterhelést [1-3].
A betegekkel kapcsolatos tényezők a következők lehetnek:
- Az NV előfordulási gyakorisága és súlyossága az elmúlt kemoterápia során. Az elmúlt kemoterápiás ciklusok során az NV-nek rossz kontrolljával rendelkező betegek valószínűleg megtapasztalják az NV-t a következő ciklusokban.
- A krónikus alkoholfogyasztás története. Azoknál a betegeknél, akiknek krónikus magas vérfelvételük van, kevésbé valószínű, hogy ciszplatinnal indukált NV-t tapasztalnak. [4]
- Kor. NV nagyobb valószínűséggel fordul elő 50 évnél fiatalabb betegeknél. [5]
- A nemek. NV nagyobb valószínűséggel fordul elő nőknél [5,6]
- A mozgásszervi betegség vagy a hányás története a terhesség alatt.
További oksági tényezők a következők lehetnek:
- Folyadék és elektrolit egyensúlytalanságok, mint a hypercalcaemia, a kötet kimerülése vagy a víz mérgezés.
- Tumor invázió vagy növekedés a gyomor-bélrendszerben, a májban vagy a központi idegrendszerben, különösen a hátsó fossa-ban.
- Székrekedés.
- Egyes gyógyszerek, mint például az opioidok.
- Fertőzés vagy szeptikémia.
- Uremia.
Az NV-t kezelő orvosoknak figyelmeztetniük kell minden lehetséges okot és tényezőt, különösen olyan rákos betegek esetében, akik több kezelés és gyógyszer kombinációját is kaphatják. (Az opioid indukálta NV-ről bővebben lásd a Rákos fájdalomról szóló PDQ-összefoglaló Opioidok című részének Káros hatások című részét.)
EUROVOC
Az NV akut, késleltetett, előretekintő, áttöréses, tűzálló és krónikusnak minősül, az alábbiak szerint: [7-9]
- Akut NV: NV, amelyet a kemoterápia beadása utáni első 24 órában tapasztaltunk, akut NV-ként kezeljük. [10]
- Késleltetett (vagy késői) NV: NV, amely a kemoterápia beadása után több mint 24 órával jelentkezik, késleltetett vagy késői NV. A késleltetett NV a ciszplatinnal, ciklofoszfamiddal és más gyógyszerekkel (például doxorubicinnel és ifoszfamiddal) kapcsolatos, nagy dózisokban vagy 2 vagy több egymást követő napon.
- Előzetes NV (ANV): Az ANV olyan émelygés és / vagy hányás, amely a kemoterápia új ciklusának megkezdése előtt megkezdődik, a kondicionált ingerekre, például a kezelés helyiségének illataira, látnivalóira és hangjaira válaszul. Az ANV egy klasszikusan kondicionált válasz, amely tipikusan három vagy négy kemoterápiás kezelés után jelentkezik, miután a beteg akut vagy késleltetett NV-t tapasztalt.
- Áttörés NV: A hányás, amely az antiemetikumok profilaktikus alkalmazásából 5 napon belül megtörténik, és mentést igényel, áttörést jelent az NV-nek.
- Tűzálló NV: NV, amely nem reagál a kezelésre.
- Krónikus NV a fejlett rákbetegekben: Az előrehaladott rákban szenvedő betegek krónikus NV-je az NV számos lehetséges etiológiához társul. Az ok végső megértése nem ismert, és nem is jól kutatott, de a potenciális ok-okozati tényezők közé tartoznak a gastrointestinalis, a cranialis, a metabolikus, a gyógyszer által kiváltott (például a morfin), a citotoxikus kemoterápia által indukált és a sugárzás által indukált mechanizmusok [11].
Irodalom
- Farrell C, Brearley SG, Pilling M és munkatársai: A kemoterápia által okozott émelygés hatása a betegek táplálkozási státuszára, pszichológiai szorongásra és életminőségre. Support Care Cancer 21 (1): 59-66, 2013. [PUBMED Abstract]
- Dranitsaris G, Bouganim N, Milano C és munkatársai: A kemoterápia által kiváltott hányinger és hányás magas kockázatú betegek azonosítására szolgáló előrejelző eszköz jövőbeni validálása. J Support Oncol 11 (1): 14-21., 2013. [PUBMED Abstract]
- Bouganim N, Dranitsaris G, Hopkins S és munkatársai: Az akut és késleltetett kemoterápia által kiváltott hányinger és hányás kockázati predikciós mutatóinak későbbi validálása. Curr Oncol 19 (6): e414-21, 2012. [PUBMED Abstract]
- Sullivan JR, Leyden MJ, Bell R: Csökkent ciszplatinnal kiváltott hányinger és hányás krónikus alkoholfogyasztással. N Engl J Med 309 (13): 796, 1983. [PUBMED Abstract]
- Tonato M, Roila F, Del Favero A: Antiemetikai vizsgálatok módszertana: áttekintés. Ann Oncol 2 (2): 107-14, 1991. [PUBMED Abstract]
- Roila F, Tonato M, Basurto C és munkatársai: Metoplopramid magas dózisainak antiemetikus aktivitása metilprednizolonnal kombinálva metoklopramiddal önmagában ciszplatinnal kezelt rákos betegekben: randomizált, kettős-vak vizsgálatot végeztek az olasz Onkológiai Csoport klinikai kutatásra. J Clin Oncol 5 (1): 141-9, 1987. [PUBMED Abstract]
- Kris MG, Urba SG, Schwartzberg LS: Klinikai kerekasztal-monográfia. A kemoterápia által kiváltott hányinger és hányás kezelése: a MASCC 2010 utáni megbeszélés. Clin Adv Hematol Oncol 9 (1): suppl 1-15, 2011. [PUBMED Abstract]
- Hesketh PJ: kemoterápia által kiváltott hányinger és hányás. N Engl J Med 358 (23): 2482-94, 2008. [PUBMED Abstract]
- Grunberg SM, Osoba D, Hesketh PJ és munkatársai: új antiemetikumok értékelése és az antineoplasztikus szer emetogenitásának meghatározása – frissítés. Support Care Cancer 13 (2): 80-4, 2005. [PUBMED Abstract]
- Wickham R: hányinger és hányás. In: Yarbo CH, Frogge MH, Goodman M, eds .: Rákos tünetek kezelése. 2. szerk. Sudbury, Mass: Jones és Bartlett Publishers, 1999, 228-263.
- Schwartzberg L: A kemoterápia által kiváltott hányinger és hányás: a legkorszerűbb technika 2006-ban. J Support Oncol 4 (2 Suppl 1): 3-8, 2006. [PUBMED Abstract]
- Nemzeti Rákkutató Intézet: A gyakori terminológiai kritériumok a nemkívánatos eseményekre (CTCAE), Version 4.0. Bethesda, Md: Amerikai Egészségügyi és Emberi Intézet, Országos Egészségügyi Intézetek, 2010. Online. Legutóbb elérte 2018. május 8-án.
Előzetes émelygés és hányás (ANV)
Előfordulás
Az ANV prevalenciája változó definíciók és értékelési módszerek miatt változott [1]. A kemoterápiában részesülő betegek kb. 29% -ánál (a három beteg közül egynek) előforduló hányinger előfordulása előfordul, míg a megelőző hányás a betegek 11% -ánál fordul elő (tíz beteg közül egy). [2] Új farmakológiai hatóanyagok bevezetésével (5-hidroxi-triptamin-3 vagy 5-HT3 receptor antagonisták), várható volt az ANV prevalenciája csökken; a vizsgálatok azonban vegyes eredményeket mutattak. Egy vizsgálat szerint az ANV alacsonyabb előfordulási aránya [3], és három vizsgálat összehasonlítható előfordulási gyakoriságot talált [2,4,5]. Úgy tűnik, hogy az 5-HT3 a szerek csökkentik a posztchemoterápiás hányást, de nem postchemoterápiás émelygést, [2,5] és az így kapott hatás az ANV-ra nem világos.
Klasszikus kondicionálás
Bár más elméleti mechanizmusokat javasoltak [6], úgy tűnik, hogy az ANV-t a klasszikus kondicionálással (Pavlovian vagy respondent kondicionálással) A klasszikus kondicionálás során egy korábban semleges inger (például a kemoterápiás környezet illatai) számos párosítás vagy tanulási kísérlet után kondicionált választ (például ANV) vált ki. A rák kemoterápiájában az első néhány kemoterápiás infúzió a tanulási kísérlet. A kemoterápiás gyógyszerek a feltétel nélküli stimulusok, amelyek kiváltják a postchemoterápia hányingert és hányást (néhány betegben). A gyógyszerek számos más, semleges, környezeti ingerrel párosulnak (például a beállítás szaga, az onkológiai nővér jelenléte, a kemoterápiás terem). Ezek a korábban semleges ingerek kondicionált ingerekké válnak és kiváltják az ANV-t a jövő kemoterápiás ciklusaiban. Az ANV nem jelzi a pszichopatológiát, hanem sokkal inkább az a tanult válasz, hogy más élethelyzetekben (például az ételmérgezésben) az adaptív elkerülést eredményezi.
Számos korrelációs tanulmány empirikus támogatást nyújt a klasszikus kondicionáláshoz. Például az ANV prevalenciája bármilyen kemoterápiás kezelés előtt nagyon ritka, és néhány betegnek valaha ANV-t tapasztalnak anamnézis utáni hemodiagnosis nélkül [8]. Továbbá, a legtöbb vizsgálat (1) nagyobb valószínűséggel találta meg az ANV-t a kemoterápiás infúziók számának növelésével, és (2) az ANV intenzitása, mivel a betegek közelebb kerülnek az infúzió tényleges idejéhez [9]. Egy kísérleti vizsgálatban kimutatták, hogy egy új ital kondicionált ingerhatáská válhat az émelygés során, ha több kemoterápiás kezeléssel párosul. [10]
Változók ANV-vel
Számos változót vizsgáltunk olyan lehetséges kockázati tényezőként, amelyek korrelálnak az ANV előfordulásával. Nincs megállapodás arról, hogy mely tényezők jelzik az ANV-t. Az alább felsorolt első nyolc jellemző közül háromnál kevesebb beteg azonban nem valószínű, hogy ANV-t alakít ki, és az első kemoterápiás infúzió után végzett szűrés meg tudja határozni a betegeket fokozott kockázat mellett [11].
Az ANV-hez kapcsolódó változók
- Életkor 50 évnél fiatalabb.
- NV az utolsó kemoterápiás kezelés után.
- Az utókezelés émelygése mérsékelt, súlyos vagy elviselhetetlen.
- Az utókezelés hányása mérsékelt, súlyos vagy elviselhetetlen.
- Az utolsó kemoterápiás kezelés után meleg vagy forróság érzi magát.
- Érzékenység a mozgásszervi betegségre.
- Női nem.
- Nagyállapotú szorongás (bizonyos helyzetekre reagáló szorongás) [12,13]
- Az autonóm idegrendszer nagyobb reaktivitása és lassabb reakcióidő. [14]
- A kemoterápia által okozott hányinger beteg elvárásai a kezelés megkezdése előtt [15,16]
- A kemoterápia infúziója, amelyet hányinger követ [17].
- Postchemoterápia szédülés.
- A post-kezelés NV későbbi késése [18]
- Különböző kemoterápiás szerek emetogén potenciálja. A post-kezelés NV közepesen súlyos vagy súlyos betegségben szenvedő betegeknél nagyobb valószínűséggel alakul ki ANV. [12]
- A reggeli betegség története a terhesség alatt.
ANV kezelése
Úgy tűnik, hogy az antiemetikus gyógyszerek nem ellenőrzik az ANV-t, ha kifejlődött [2], azonban számos viselkedési beavatkozást vizsgáltunk [19] Ezek a következők:
- Progresszív izomlazulás vezetett képekkel. [20]
- Hipnózis. [21]
- Szisztematikus deszenzitizáció [22]
- Elektromiográfia és termikus biofeedback [23]
- Megtorlás videojátékok használatával [24,25]
Progresszív izomlazítást irányított képekkel, hipnózissal és szisztematikus deszenzitizációval vizsgálták a legtöbbet, és kezelésnek tekintendők. Az ANV azonosítása során figyelembe kell venni a pszichológushoz vagy más mentális egészségügyi szakemberhez való eljuttatást, ahol speciális képzés és tapasztalat van a rákbetegek kezelésében. A korábbi ANV-t azonosítják, annál valószínűbb a kezelés hatékonyabb; így a korai szűrés és az áttétel elengedhetetlen. Az orvosok és az ápolónők azonban alábecsülik a kemoterápia által indukált NV hatását. [26] [A bizonyítékok szintje: II]
Nyilvánvaló, hogy az ANV legfontosabb szempontja a kemoterápiával kapcsolatos akut és késleltetett NV megelőzése. A legtöbb antiemetik nem mutatott hasznot az ANV kezelésére, de az antiemetikumok alkalmazása a kemoterápia során drámai hatással lehet az ANV előfordulási gyakoriságának csökkentésére. Az egyetlen gyógyszerosztály, amely bizonyos vizsgálatokban előnyösnek bizonyult, a benzodiazepinek, leggyakrabban lorazepám. [27] [Bizonyítékok szintje: IV]
Irodalom
- Andrykowski MA: Előzetes hányinger és hányás meghatározása: különbségek a rákos kemoterápiás betegek között, akik előzetesen kezelik a hányingert. J Behav Med 11 (1): 59-69, 1988. [PUBMED Abstract]
- Morrow GR, Roscoe JA, Kirshner JJ és munkatársai: Előzetes hányinger és hányás az 5-HT3 antiemetikum korában. Support Care Cancer 6 (3): 244-7, 1998. [PUBMED Abstract]
- Aapro MS, Kirchner V, Terrey JP: Előzetes hányinger és hányás előfordulása ismételt ciklusú kemoterápia után: a granisetron hatása. Br J Cancer 69 (5): 957-60, 1994. [PUBMED Abstract]
- Fernández-Marcos A, Martín M, Sanchez JJ és munkatársai: Akut és megelőző hányás mellrákos betegeknél. Support Care Cancer 4 (5): 370-7, 1996. [PUBMED Abstract]
- Roscoe JA, Morrow GR, Hickok JT és munkatársai: Hányinger és hányás továbbra is jelentős klinikai probléma: időbeli trendek a kemoterápia által kiváltott hányinger és hányás megelőzésében 1413, közösségi klinikai gyakorlatban kezelt betegben. J Pain Symptom Manage 20 (2): 113-21, 2000. [PUBMED Abstract]
- Reesal RT, Bajramovic H, Mai F: Előzetes hányinger és hányás: kemoterápia fóbia formája? Can J Psychiatry 35 (1): 80-2, 1990. [PUBMED Abstract]
- Stockhorst U, Klosterhalfen S, Steingruber HJ: Kondicionált hányinger és további mellékhatások a rák kemoterápiában: felülvizsgálat. Journal of Psychophysiology 12 (suppl 1): 14-33, 1998.
- Morrow GR, Rosenthal SN: Modellek, mechanizmusok és megelőző hányinger és hányás kezelése. Oncology 53 (Suppl 1): 4-7, 1996. [PUBMED Abstract]
- Montgomery GH, Bovbjerg DH: Előzetes hányinger kialakulása emlőcarcinomában adjuváns kemoterápiát kapó betegeknél. Physiol Behav 61 (5): 737-41, 1997. [PUBMED Abstract]
- Bovbjerg DH, Redd WH, Jacobsen PB és munkatársai: A klasszikusan kondicionált hányinger kísérleti elemzése a rák kemoterápia során. Psychosom Med 54 (6): 623-37, 1992 nov-dec. [PUBMED Abstract]
- Morrow GR, Roscoe JA, Hickok JT: Hányinger és hányás. In: Holland JC, Breitbart W, Jacobsen PB és munkatársai, szerk .: Pszicho-onkológia. New York, NY: Oxford University Press, 1998, 476-484.
- Andrykowski MA, Redd WH, Hatfield AK: Előzetes émelygés kifejlesztése: prospektív elemzés. J Consult Clin Psychol 53 (4): 447-54, 1985. [PUBMED Abstract]
- Roscoe JA, Morrow GR, Hickok JT és munkatársai: Bio-viselkedési tényezők a kemoterápia által kiváltott hányinger és hányás során. J Natl Compr Canc Netw 2 (5): 501-8, 2004. [PUBMED Abstract]
- Kvale G, Psychol C, Hugdahl K: Kardiovaszkuláris kondicionálás és megelőző hányinger és hányás rákos betegekben. Behav Med 20 (2): 78-83, 1994 Nyár. [PUBMED Abstract]
- Montgomery GH, Tomoyasu N, Bovbjerg DH és munkatársai: A betegek kemoterápiával kapcsolatos émelygés előtti elvárásai a megelőző hányinger független előrejelzői. Ann Behav Med 20 (2): 104-9, 1998 Tavasz. [PUBMED Abstract]
- Shelke AR, Roscoe JA, Morrow GR és munkatársai: Émelygés-várakozás manipulációjának hatása a kemoterápia által kiváltott hányingerre: a Rochester-i rákközpont közösségi klinikai onkológiai programja. J Pain Symptom Manage 35 (4): 381-7, 2008. [PUBMED Abstract]
- Tomoyasu N, Bovbjerg DH, Jacobsen PB: A rákos kemoterápiára kifejtett reakciók: a százalékos erősítés előrejelző hányingert jelez. Physiol Behav 59 (2): 273-6, 1996. [PUBMED Abstract]
- Chin SB, Kucuk O, Peterson R és munkatársai: A rákos kemoterápiában előzetesen hányinger és hányás elősegítő változók. Am J Clin Oncol 15 (3): 262-7, 1992. [PUBMED Abstract]
- Carey MP, Burish TG: A rák kemoterápiájával kapcsolatos pszichológiai mellékhatások etiológiája és kezelése: kritikai áttekintés és vita. Psychol Bull 104 (3): 307-25, 1988. [PUBMED Abstract]
- Lyles JN, Burish TG, Krozely MG és munkatársai: A relaxációs tréning hatékonysága és a vezetett képalkotás a rák kemoterápiás érzékenységének csökkentésében. J Consult Clin Psychol 50 (4): 509-24, 1982. [PUBMED Abstract]
- Redd WH, Andresen GV, Minagawa RY: A rákos kemoterápiában részesülő betegek előretekintő hányásának hipnózisos kontrollja. J Consult Clin Psychol 50 (1): 14-9, 1982. [PUBMED Abstract]
- Morrow GR, Morrell C: viselkedésbeli kezelés a rákos kemoterápia által indukált hányinger és hányás megelőzésére. N Engl J Med 307 (24): 1476-80, 1982. [PUBMED Abstract]
- Burst TG, Shartner CD, Lyles JN: A többszörös izomhelyi EMG biofeedback és relaxációs tréning hatékonysága a rák kemoterápiás érzékenységének csökkentésében. Biofeedback Self Regul 6 (4): 523-35, 1981. [PUBMED Abstract]
- Kolko DJ, Rickard-Figueroa JL: A videojátékok hatása a kemoterápia káros következményeire a gyermekgyógyászati onkológiai betegeken: egyszeri analízis. J Consult Clin Psychol 53 (2): 223-8, 1985. [PUBMED Abstract]
- Vasterling J, Jenkins RA, Tope DM és munkatársai: Kognitív distrakciós és relaxációs tréning a rákkemoterápia miatti mellékhatások szabályozására. J Behav Med 16 (1): 65-80, 1993. [PUBMED Abstract]
- Chan CW, Cheng KK, Lam LW és munkatársai: pszicho-oktatási beavatkozás kemoterápiával kapcsolatos hányinger és hányás gyermekgyógyászati onkológiai betegeknél: kísérleti vizsgálat. Hong Kong Med J 14 (5 Suppl): 32-5, 2008. [PUBMED Abstract]
- Rock EM, Limebeer CL, Parker LA: Előzetes hányinger állatmodellekben: a lehetséges új terápiás kezelések áttekintése. Exp Brain Res 232 (8): 2511-34, 2014. [PUBMED Abstract]
Akut vagy késleltetett kemoterápia által kiváltott hányinger és hányás (NV) etiológiája
Az akut NV közepes vagy magas rizikójú kemoterápiában bekövetkező incidenciája 30% -tól 90% -ig terjed. [1-3] Jelentős megbetegedésekhez vezethet, és negatívan befolyásolhatja az életminőséget. Az elmúlt években azonban számos új antiemetikus gyógyszer és kombináció vált elérhetővé, ami drámai módon csökkenti a rettegett szövődmény incidenciáját és súlyosságát. A kockázati tényezők közé tartozik az adott hatóanyag emetogén potenciálja, az alkalmazott dózis, a kezelési ütemterv és a kemoterápiás szerek kombinálása. Például egy alacsony dózisú emetogén potenciállal rendelkező gyógyszer drámai módon növelheti az NV indukálódásának lehetőségét [4]. A cytarabin standard dózisai ritkán állítják elő az NV-t, de az NV gyakran előfordul a nagy dózisú gyógyszerrel. Egy másik befolyásoló tényező a kábítószer-kombinációk alkalmazása. Mivel a legtöbb beteg kombinált kemoterápiát kap, az összes gyógyszer emetogén potenciálját és az egyes gyógyszeradagokat meg kell fontolni. [5-9]
Egyéb kockázati tényezők a következők: [10]
- Gyenge kontroll a korábbi kemoterápiával.
- Női nem.
- Életkor 50 évnél fiatalabb.
- Tapasztalatok az előző kemoterápiával.
- A mozgássérültség története.
- A terhesség indukálta NV története.
- Kiszáradás.
- Alultápláltság.
- Legutóbbi műtét.
- Sugárkezelés.
Az American Society of Clinical Oncology kidolgozta a kemoterápiás szerek minősítési rendszerét és az akut és késleltetett hányás kockázatát [10].
- Nagy kockázat: A hányás, amelyet a betegek több mint 90% -ában dokumentáltak:
- Carmustine.
- Cisplatin.
- Ciklopofoszfamid (≥ 1500 mg / m2).
- Dacarbazine.
- Dactinomicínt.
- Mekloretamin.
- Streptosotocinnal.
- Alemtuzumab.
- Azacitidin.
- Bendamusztin.
- Carboplatin.
- Klofarabin.
- Ciklopofoszfamid (
Késleltetett NV
A késleltetett (vagy késői) NV a kemoterápia beadása után több mint 24 órával jelentkezik. A késleltetett NV a ciszplatinnal, ciklofoszfamiddal és más gyógyszerekkel (például doxorubicinnel és ifoszfamiddal) kapcsolatos, nagy dózisokban vagy két vagy több egymást követő napon adva [1,11,12]
- etiológiák:
- Azok a betegek, akik kemoterápiás akut hányást tapasztalnak, sokkal nagyobb valószínűséggel késlelteti a hányást.
- Az akut hányás minden prediktív jellemzőjét a késleltetett hányás rizikófaktorainak tekintjük.
- További információt az összefoglaló Acute Nausea and Hatching (NV) részében talál.
Irodalom
- Hesketh PJ, Sanz-Altamira P, Bushey J és munkatársai: A késői émelygés és hányás incidenciája az oxaliplatin alapú kemoterápiában részesülő vastagbélrákos betegeknél. Support Care Cancer 20 (5): 1043-7, 2012. [PUBMED Abstract]
- Schwartzberg L: Az új terápiák értékének kezelése a kemoterápia által kiváltott hányinger és hányás során. Expert Rev Pharmacoecon Outcomes Res 14 (6): 825-34, 2014. [PUBMED Abstract]
- Sekine I, Segawa Y, Kubota K és munkatársai: A kemoterápia által kiváltott hányinger és hányás kockázati tényezői: index személyre szabott antiemetikus profilaxisra. Cancer Sci 104 (6): 711-7, 2013. [PUBMED Abstract]
- Roscoe JA, Morrow GR, Hickok JT és munkatársai: Hányinger és hányás továbbra is jelentős klinikai probléma: időbeli trendek a kemoterápia által kiváltott hányinger és hányás megelőzésében 1413, közösségi klinikai gyakorlatban kezelt betegben. J Pain Symptom Manage 20 (2): 113-21, 2000. [PUBMED Abstract]
- Viale PH, Grande C, Moore S: Hatásosság és költség: a kemoterápia által kiváltott hányinger és hányás elkerülése. Clin J Oncol Nurs 16 (4): E133-41, 2012. [PUBMED Abstract]
- Dranitsaris G, Bouganim N, Milano C és munkatársai: A kemoterápia által kiváltott hányinger és hányás magas kockázatú betegek azonosítására szolgáló előrejelző eszköz jövőbeni validálása. J Support Oncol 11 (1): 14-21., 2013. [PUBMED Abstract]
- Kris MG, Urba SG, Schwartzberg LS: Klinikai kerekasztal-monográfia. A kemoterápia által kiváltott hányinger és hányás kezelése: a MASCC 2010 utáni megbeszélés. Clin Adv Hematol Oncol 9 (1): suppl 1-15, 2011. [PUBMED Abstract]
- Phillips RS, Gopaul S, Gibson F és munkatársai: Antiemetikus gyógyszerek a kemoterápia által kiváltott hányinger és hányás megelőzésére és kezelésére gyermekkorban. Cochrane Database Syst Rev (9): CD007786, 2010. [PUBMED Abstract]
- Olver I, Clark-Snow RA, Ballatori E és munkatársai: Hányinger és hányás szabályozására vonatkozó iránymutatás alacsony vagy minimális hányáspotenciálú kemoterápiával. Support Care Cancer 19 (Suppl 1): S33-6, 2011. [PUBMED Abstract]
- Kris MG, Hesketh PJ, Somerfield MR és munkatársai: American Society of Clinical Oncology: antiemetikum oncology: update 2006. J Clin Oncol 24 (18): 2932-47, 2006. [PUBMED Abstract]
- Geling O, Eichler HG: Az 5-hidroxi-triptamin-3 receptor antagonistákat a kemoterápia után 24 órával kell beadni a késleltetett hányás megelőzésére? A klinikai bizonyítékok és a gyógyszerköltségek következményeinek szisztematikus újraértékelése. J Clin Oncol 23 (6): 1289-94, 2005. [PUBMED Abstract]
- Fleishman SB, Mahajan D, Rosenwald V és munkatársai: késleltetett hányinger és / vagy hányás előfordulása oxaliplatin alapú regisztrátumokkal kezelt betegek számára a colorectalis rák kezelésére. J Oncol Pract 8 (3): 136-40, 2012. [PUBMED Abstract]
Akut vagy késleltetett hányinger és hányás megelőzése és kezelése
Számos szervezet – köztük az American Society of Clinical Oncology, az Országos Átfogó Rákellenes Hálózat és az Ontario Pediatric Oncology Group – megjelentek antiemetikus irányvonalakat tagjaik számára. A PDQ politikája nem a konkrét iránymutatások elfogadására irányul, de példák találhatók a szakirodalomban. [1-4]
Az antiemetikus szerek a leggyakoribb beavatkozás a kezeléssel összefüggő NV kezelésében. Az antiemetikus terápia alapja a hányás neurokémiai szabályozása. Bár a pontos mechanizmust nem értik jól, a perifériás neuroreceptorok és a kemooreceptor-trigger zóna (CTZ) ismert szerotonin, hisztamin (H1 és H2), dopamin, acetilkolin, opioidok és számos más endogén neurotranszmitter receptorait tartalmazzák [5,6 ] Számos antiemetikum gátolja a receptorok kompetitív blokkolását ezeknek az anyagoknak, ezáltal gátolja a perifériás idegek stimulálását a CTZ-ben és esetleg a hányásközpontban.
Közepesen emetogén kemoterápiában részesülő betegeknél az 5-HT kombinációja3 receptor antagonistát és a dexametazont predekterápia formájában alkalmazzák lorazepámmal vagy anélkül. Az antraciklin és a ciklofoszfamid kombinációját kapó betegek és olyan betegek kiválasztása, akik más, mérsékelt emetikus kockázattal rendelkező szereket is kapnak, mint pl. A ciszplatin (2. táblázat. Antiemetikus ajánlások emetikus kockázati kategóriák szerint
fenotiazinok
A fenotiazinok hatással vannak a dopaminerg receptorokra a CTZ-ben, esetleg más központi idegrendszeri (CNS) központokban és perifériásan.
A fenotiiazinok kiválasztásának elsődleges szempontja a káros hatásprofilok különbsége, amelyek összefüggenek a strukturális osztályukkal. Általában az alifás fenotiazinok (pl. A klórpromazin) szedálást és antikolinerg hatásokat termelnek, míg a piperazinok (pl. Proklorperazin) kevésbé nyugtató hatásúak, de az extrapiramidális tünetek (EPS) (akut dystoniák, akathisia, neuroleptikus malignus szindróma [nem gyakori] , ritkán akinesia és dyskinesia). Jelentős hipotenzió akkor is kialakulhat, ha IV dózisokat adnak be gyorsan nagy adagokban. A H1-blokkolók, mint például a difenohidramin egyidejű alkalmazása gyakran csökkenti az EPS rizikóját és súlyosságát. A fenotiazinok különösen értékesek lehetnek azoknál a betegeknél, akik a késői NV-t ciszplatin-kezelésben szenvednek [25-29] [A bizonyítékok szintje: I] Antikolinerg tulajdonságaik miatt a fenotiazinok szerepelnek az American Geriatrics Society Beers kritériumai között a potenciálisan nem megfelelő gyógyszeres kezeléshez Idősebb felnőttek. [30]
butirofenonok
A droperidol és a haloperidol butirofenonok, a dopaminerg (D2 altípus) receptor antagonisták, amelyek szerkezetileg és farmakológiai szempontból hasonlóak a fenotiiazinokhoz. Bár a droperidolt elsősorban az anesztézia indukciójának kiegészítéseként alkalmazzák, a haloperidol neuroleptikus antipszichotikumként szerepel; mindkét hatóanyagnak van valamilyen antiemetikus hatása. A droperidolt tipikusan 1 mg-tól 2,5 mg-ig IM vagy IV-be adják 2-6 óránként, de nagyobb adagok (legfeljebb 10 mg) biztonságosan adhatók [31,32] A haloperidolt tipikusan 1 mg-tól 4 mg-ig adják be, IV, vagy orálisan, minden 2-6 órában. [33] Egy kis, ellenőrizetlen, nyílt klinikai vizsgálat eredményei a pallátozisban szenvedő betegeknél bizonyos hatékonyságot mutattak a haloperidol esetében [34]. Mindkét hatóanyag EPS, akathisia, hypotensio és szedáció lehet.
Olanzapin
Az olanzapin antipszichotikum a thienobenzodiazepin gyógyszerosztályban, amely blokkolja a neurotranszmittereket: a dopamin D-ben1, D2, D3, és D4 agyi receptorok; szerotonin 5-HT-nél2a, 5-HT2c, 5-HT3, és az 5-HT6 receptorok; katecholaminok alfa-1 adrenerg receptorokon; acetilkolin muszkarin receptorokon; és hisztamin H-ban1 receptorok. [35] A gyakori mellékhatások a következők: [36,37]
- Nyugtatás.
- Száraz száj.
- Fokozott étvágy.
- Hízás.
- Testtartás által bekövetkezett vérnyomáscsökkenés.
- Szédülés.
Az olanzapin több receptorra gyakorolt hatása, különösen a D2 és az 5-HT3 amelyek úgy tűnik, hogy részt vesznek az NV-ben, azt sugallja, hogy jelentős antiemetikus tulajdonságokkal rendelkezhet. [38] [Bizonyítékok szintje: II] A későbbi vizsgálatok kimutatták az olanzapin CINV antiemetikum hatékonyságát [39,40] : II] Egy nagy tanulmány [41] [A bizonyítékok szintje: I] kimutatta, hogy a magas emetogén kemoterápiában vagy közepesen emetogén kemoterápiában részesülő betegeknél az azazetron és a dexamethason hozzáadása az olanzapin hozzáadásával javította a késleltetett CINV teljes válaszát (CR).
Egy véletlenszerű, kettős vak III. Fázisú vizsgálatban az olanzapin és a placebo mellett a magas emetogén kemoterápiával járó CINV megelőzésére alkalmazott standard antiemetikumok értékelték. [20] [Bizonyítékok szintje: I] A legalább ciszplatinnal kezelt, kemoterápiával nem kezelt betegek mg / m 2 testtömeg (BSA) kiegészítő szerekkel vagy anélkül, vagy a 60 mg / m2 dxorubicin BSA-val és 600 mg / m2 BSA ciklofoszfamiddal véletlenszerűen 10 mg orális adagot kaptak orálisan az 1-4. napokon vagy a placebóval egyező, iránymutatással irányított antiemetikumokkal. Az antiemetikus kezelés magában foglalja az NK-1 antagonistát (foszaprepitant vagy aprepitant), az 5-HT3 (palonosetron, granisetron vagy ondansetron) és az első napon 12 mg dexametazon, majd a napi 2 mg-os napi 8 mg-os orális adagolás után. A betegeket szexuális, kemoterápiás és specifikus 5-HT3 antagonista. Az elsődleges végpontot, hányingert nem, a 0-tól 10-ig terjedő vizuális analóg skála szerint 0-as pontszámként definiálták és három időpontban értékelték a poszt-kezelést: korai, 0-24 óra; később, 25-120 óra; és összességében 0-120 óra.
Az émelygéses betegek aránya szignifikánsan magasabb volt az olanzapin csoportban, mint korábban a placebo csoportban (74% vs. 45%, P = .002), később (42% vs. 25%, P = .002), és a teljes időponthoz (37% vs. 22%, P = .002). A CR (nincs hányás, nem mentőképesség) és a klinikailag jelentős hányingertől (3-nál alacsonyabb pontszám a vizuális analóg skálán 0-10) szignifikánsan javult az olanzapin adagolásával minden időpontban. Az olanzapinnal kezelt betegeknél a 2. naptól kezdődően fokozódott a szedáció a kiindulási értékről, amely a 3-5. Napokon oldódott. Ezen adatok és további klinikai vizsgálatok alapján az olanzapin biztonságos és hatásosnak bizonyult az akut és késleltetett CINV kezelésében azoknál a betegeknél, akik nagyon emetogén és mérsékelten emetogén kemoterápia [42,43]
Helyettesített benzamidok
A metoklopramid egy szubsztituált benzamid, amely a szerotonin (5-HT3) receptor antagonistákat vezettek be, a legmagasabb emetogén kemoterápia elleni hatékony antiemetikumnak tekintették. Bár a metoklopramid kompetitív antagonista a dopaminerg (D2) receptorok esetében a leghatásosabb az akut hányás ellen, amikor IV-t adnak nagy dózisokban, valószínűleg azért, mert gyenge versenyképes antagonista (más szerotonin antagonistákhoz képest) az 5-HT3 receptorokhoz. A CTZ-re és a perifériára is hatással lehet. A metoklopramid szintén növeli az alsó nyelőcső sphincter nyomását, és fokozza a gyomorürülés sebességét, ami a teljes antiemetikus hatását befolyásolhatja. A metoklopramidot biztonságosan adták IV bolus injekcióval nagyobb egyszeri dózisokban (legfeljebb 6 mg / kg) és folyamatos IV infúzióval, terheléses bolus dózissal vagy anélkül, a hatékonysággal összehasonlítva a többszörös intervallumos adagolási rendekkel [44- 46]
A metoklopramid akathisia és dystonic EPS-hez társul; Az akathisia gyakrabban fordul elő 30 évnél idősebb betegeknél, és a dystoniás EPS gyakrabban fordul elő 30 évnél fiatalabb betegeknél. A difenhidramin, a benztropin-mezilát és a trihexifenidil általánosan profilaxiás vagy terápiásan alkalmazzák az EPS-t farmakológiai szempontból antagonizálva. [47] Míg a fogaskerék merevsége, akut dystonia és remegés reagál az antikolinerg gyógyszerekkel, az akathisia kezelést a metoklopramid dózisának csökkentésével, egy másik hatóanyagra vagy benzodiazepin hozzáadásával lehet kezelni.
Úgy gondolják, hogy a trimetohobenzamid központilag hat a CTZ-ben a hányásimpulzusok blokkolásával. Korlátozott számú onkológiai betegen tanulmányozták a hányingert különböző kemoterápiás kezelésekből. A placebóval összehasonlítva a trimetohobenzamid 200 mg IM 6 óránként 2 napra jelentősen csökkentette az émelygést és a hányást. [18]
5-HT3 Receptor antagonisták
Négy szerotonin receptor antagonista-ondansetron, granisetron, dolasetron és palonosetron áll rendelkezésre az Egyesült Államokban. A Tropisetron, bár az amerikai FDA (Food and Drug Administration) nem hagyja jóvá, más országokban is elérhető. Az ebbe az osztályba tartozó hatóanyagokat úgy gondolják, hogy megakadályozzák az NV-t a gastrointestinalis (GI) nyálkahártya enterochromaffin sejtjeiből felszabaduló szerotonin megakadályozásával az afferens átvitelnek a központi idegrendszerbe történő indításával a vagális és spinalis szimpatikus idegeken [48-50] Az 5-HT3 receptor antagonisták blokkolhatják a szerotonin stimulációt a CTZ és más CNS struktúrákban. A gyógyszerek ezen osztályának főbb mellékhatásai közé tartozik az enyhe fejfájás és a székrekedés. Több tanulmány kimutatta, hogy az 5-HT3 receptor antagonisták a leghatékonyabbak, ha szteroidokkal együtt adják.
Az anyagok összehasonlítása
A vizsgálatok szerint a három első generációs 5-HT hatékonysága vagy toxicitása között nincs jelentős különbség3 receptor antagonisták (dolasetron, granisetron és ondansetron) az akut CINV kezelésében. Ez a három szer egyenértékű hatékonysággal és toxicitással, ha megfelelő dózisokban alkalmazzák [51,52]; [53] [A bizonyítékok szintje: I] Bár ezek az anyagok kimutatták, hogy hatásosak az első 24 órában posztkémiai kezelésben (akut fázisban), nem igazolták, hogy hatásosak a 2-5. Napon a posztkémia (késleltetett fázis) után.
Palonosetron, a második generációs 5-HT3 receptor antagonistát, erősen és mérsékelten emetogén kemoterápiában szenvedő akut hányás szabályozására engedélyezték, és mérsékelten emetogén kemoterápiát kapó betegeknél késleltetett hányás jóváhagyására [54]; [55] [A bizonyítékok szintje: I]
Az első generációs és a második generációs 5-HT használatának ellenére3 receptor antagonisták, az akut CINV és különösen a késleltetett NV szabályozása szuboptimális, és jelentős lehetőségek állnak rendelkezésünkre új hatóanyagok hozzáadásával vagy helyettesítésével a jelenlegi kezelésekben [9,56-58]
Az ondanszetron
Számos tanulmány kimutatta, hogy az ondansetron olyan antiemetikus válaszreakciót eredményez, amely nagyobb vagy nagyobb a metoklopramid dózisainakéhoz képest, de az ondanszetron javított toxicitási profillal rendelkezik, szemben a dopaminerg antagonista hatóanyagokkal. [59-62] [A bizonyítékok szintje: I ] [63,64] Az ondansetront (0,15 mg / kg IV) 15-30 perccel a kemoterápia előtt adják be, és két további adag után 4 óránként megismételve. A ciszplatin randomizált vizsgálata nem talált különbséget a 8 mg-os és a 32 mg-os dózisok között [65]. Az egyközpontú retrospektív térkép áttekintést jelentett a napi 16 mg / m2 IV (maximum 24 mg) ondanszetron feltöltődésről csecsemők, gyermekek és serdülők számára. [66] Azonban az FDA-nak bejelentett adatok aggodalmukat fejezték ki a QT-megnyúlással és esetlegesen halálos aritmiákkal kapcsolatban egyetlen 32 mg-os IV-dózissal kapcsolatban. A jelenlegi gyógyszercímkézés egy maximális 16 mg-os IV dózist igényel [67].
Jelenleg az orális és injektálható ondansetron készítmények 4 évesnél idősebb betegeknél, beleértve az idős betegeket és veseelégtelenségben szenvedő betegeket, dózismódosítás nélkül használják fel. Az orális ondansetront naponta 3 alkalommal adják be a kemoterápia előtt 30 perccel, és a kemoterápia befejezése után legfeljebb 2 napig tartanak. Az ondansetron clearance csökken súlyos májelégtelenségben szenvedő betegeknél; ezért ezeknél a betegeknél egyetlen injekciós vagy orális dózis nem haladja meg a 8 mg-ot. Jelenleg nincs információ az ismételt napi ondansetron dózisok biztonságosságáról a májelégtelenségben szenvedő betegeknél. Más hatékony adagolási rendeket is értékeltek, mint például egy folyamatos IV infúzió (például 1 mg / óra 24 óra) vagy orális beadás. [68]
Az ondansetron főbb mellékhatásai a következők: [69]
- Fejfájás (enyhén fájdalomcsillapító hatású).
- Székrekedés.
- Fáradtság.
- Száraz száj.
- A májfunkciós tesztek átmeneti tünetmentes emelkedése (alanin és aszpartát transzaminázok), amelyek összefüggésben lehetnek a ciszplatin egyidejű alkalmazásával.
Az ondansetron etiológiailag érintett néhány esettanulmányban, amelyek thrombocytopeniát, veseelégtelenséget és thromboticus eseményeket érintettek [70]. Az ritka elektrokardiogram változása QTc-megnyúlás formájában jelentkezhet. Ezenkívül néhány esetjelentés az ondanszetront érintette az EPS okozásával. Bizonyos esetekben azonban nem világos, hogy a leírt események ténylegesen EPS-k voltak-e; más jelentésekben a bizonyítékokat megzavarják az egyéb olyan szerek egyidejű alkalmazásával, amelyek ismert módon EPS-t termelnek. Mindazonáltal a szerotonin receptor antagonisták legnagyobb előnye a dopaminerg receptor antagonistákkal szemben, hogy kevesebb káros hatásuk van. Az ondansetron profilaxis ellenére sok doxorubicint, ciszplatint vagy karboplatint kapó beteg akut és késleltetett fázisú NV-t tapasztal. [71] Egy randomizált, kettős-vak, placebo-kontrollos vizsgálat azt mutatta, hogy az aprepitant, az NK-1 receptor antagonistája, enyhítheti az NV-t [72,73] [A bizonyítékok szintje: I]
Granisetron
Mind a granisetron készítmények, mind az ondansetron injekció ugyanazt a jelzést hordozza a magas emetogén kemoterápia ellen. Ezzel szemben az orális ondansetron készítmény csak a mérsékelten emetogén kemoterápiához társult NV ellen használható.
Jelenleg a granisetron injekciót 2 évesnél idősebb betegeknél, beleértve az idős betegeket és a máj- és veseelégtelenségben szenvedő betegeket, dózismódosítás nélkül engedélyezték.
dolasetront
A dolasetron orális készítményei mérsékelten emetogén rákos kemoterápiához társuló NV megelőzésére szolgálnak, ideértve a kezdeti és ismétlődő tanfolyamokat is. Az orális dolasetron a kemoterápia előtt 1 órával 100 mg-os dózisban adagolható. A Dolasetron-t IV vagy orálisan 1,8 mg / ttkg dózisban adagolták egyetlen adagban körülbelül 30 perccel a kemoterápia előtt. Az injekciós készítmények azonban már nem engedélyezettek a CINV számára a QTc intervallum megnyúlásának kockázata miatt [75].
A orális dolasetron hatékonysága a CINV megelőzésére 399 beteg nagy randomizált, kettős-vak, összehasonlító vizsgálata során bizonyítást nyert. [76] [Bizonyítékok szintje: I] A szájon át alkalmazott dolasetron 25-200 mg 1 órával a kemoterápia előtt. A másik vizsgálati ág a szájon át beadott ondansetron (8 mg) volt, amelyet a kemoterápia előtt 1,5 órával és a kemoterápia után 8 óránként összesen három dózisban adtak be. A CR-értékek (amelyeket úgy határoznak meg, hogy nincs hányás epizód és a menekülési antiemetikus gyógyszerek használata) nem javultak a növekvő dolasetron dózisokkal. Mind a dolasetron 200 mg, mind az ondansetron szignifikánsan magasabb CR-értéket mutatott, mint a dolasetron 25 vagy 50 mg.
Palonosetron
A palonosetron egy 5-HT3 receptor antagonista (második generáció), amely antiemetikus aktivitást mutat mind központi, mind GI helyeken. A Palonosetron az FDA jóváhagyása a mérsékelt és magas emetogén rák kemoterápia kezdeti és ismétlődő tanfolyamaihoz társuló akut NV megelőzésére és a mérsékelten emetogén rákos kemoterápia kezdeti és ismétlődő tanfolyamaira vonatkozó késleltetett NV megelőzésére. Összehasonlítva a régebbi 5-HT-vel3 receptor antagonisták, a palonosetron nagyobb kötődési affinitást mutat az 5-HT-hez3 receptorok, nagyobb hatékonyság, szignifikánsan hosszabb felezési idő (körülbelül 40 óra, 4-5-ször hosszabb, mint a dolasetron, granisetron vagy ondansetron) és kiváló biztonsági profil. [77] [Bizonyítékok szintje: I] A dózisfelvételes vizsgálat kimutatta, hogy a hatásos dózis 0,25 mg vagy annál magasabb volt [78-82]
A mérsékelten emetogén kemoterápiát kapó betegek két nagy vizsgálata során a CR (hányás, mentés nélkül) szignifikánsan javult az akut és késleltetett időszakokban azoknál a betegeknél, akik 0,25 mg palonosetront önmagában kaptak, szemben az ondansetronnal vagy a dolasetronnal önmagában [54]; [55] [A bizonyítékok szintje: I] A dexametazont nem adták az 5-HT-vel3 receptor antagonisták, és még nem ismert, hogy a CR különbségek továbbra is fennmaradnak-e, ha dexametazont használnak. Egy másik vizsgálatban [Disease: I] 650 emetogén kemoterápiában részesülő (cisplatin ≥60 mg / m 2) dessametazont és egy vagy két dózisú palonosetron (0,25 mg vagy 0,75 mg) vagy dexametazon ondansetron (32 mg). Az egyadagos palonoszetron ugyanolyan hatásos volt, mint az ondansetron az akut CINV dexametazon előkezelésének megelőzésére; szignifikánsan hatékonyabb volt, mint az ondansetron az 5 napos posztkémiai kezelés alatt. A fenti vizsgálatokban részesülő betegek analízisében, akik ismételt kemoterápiás ciklusokat kaptak, egy szerző [84] arról számolt be, hogy mind az akut, mind a késői CINV esetében a CR-értékeket egyszeri IV-es palonosetron-dózisban tartották anatómiai kortikoszteroidok nélkül.
NK-1 receptor antagonisták (P szubsztancia antagonisták)
A nucleus tractus solitarius vagus afferens neuronjaiban, a hasi vagusban és a postrema területen található P anyag, hányást vált ki. NK-1 receptor antagonisták, ideértve az aprepitantot, a foszaprepitantot, a netupitant és a robbantást elősegítő P-blokk-anyagot az NK-1-receptorhoz történő kötődéshez. 5-HT-vel kombinálva3 receptor antagonista és kortikoszteroid, az NK-1 receptor antagonisták az akut és késleltetett NV megelőzésére javalltok, amely a magas és mérsékelten emetogén kemoterápia kezdeti és ismétlődő szakaszaihoz kapcsolódik.
Aprepitant / foszaprepitanttal
Klinikai vizsgálatok [85-88] kimutatták, hogy az aprepitant hozzáadása 5-HT-hez3 receptor antagonista és dexametazon a ciszplatin kemoterápia előtt javította az akut hányás szabályozását, összehasonlítva egy 5-HT3 receptor antagonista és dexametazon; ez a rendszer javította a késleltetett hányás szabályozását a placebóhoz képest. Két randomizált, kettős-vak, párhuzamos, kontrollos vizsgálatban a betegek ciszplatint (≥70 mg / m 2) kaptak, és véletlen besorolással kaptak standard terápiát az ondansetronnal és a dexametazon prechemoterápiával és a dexametazonnal a posztchemoterápia 2-4. vagy a standard terápia és az aprepitant prechemoterápia, valamint a 2. és 3. napon. [89,90] [Bizonyítékok szintje: I] Mindkét vizsgálatnál az aprepitant csoport CR (nincs hányás, nem mentés) szignifikánsan magasabb volt mind az akut, mind a késleltetett időszakok. Egy további vizsgálat megerősítette az aprepitant hatékonyságát a késleltetett időszakban, amikor az ondansetronnal hasonlították össze. [91] [A bizonyítékok szintje: I]
Az aprepitant előnyeit a magas emetogén kemoterápia mellett mutatták ki. Az aprepitantnak az ondansetronra és a dexametazonra gyakorolt hatása az enyhe emetogén kemoterápia és az ondansetron és a dexametazon önmagában történő alkalmazása előtt jobb CINV kimeneteket eredményezett [92-94] Egy alternatív adagolási stratégiát értékeltek egy randomizált, kettős-vak, placebo-kontrollos, akik 5 napos ciszplatin kombinációs kemoterápiát kaptak csírasejtes daganatokban [95]. A szokásos antiemetikus terápia mellett a betegek a 3. napon aprepitantot kaptak 125 mg-mal, majd a 4-7. Napokon 80 mg aprepitantot kaptak. A CINV CR jelentősen javult a három gyógyszeres kezeléssel.
A aprepitant vízoldható, foszforilált analógja, a fozaprepitant dimeglumint gyorsan átváltoztatják aprepitantra IV adagolás után [96]. A kemoterápiát megelőzően a fosaprepitant 150 mg-os egyszeri adagban, a 3 napos orális aprepitant-kezelés alternatívájaként engedélyezett. A ciszplatin kemoterápiát kapó betegek randomizált, kettős vak vakcinációjában kimutatták, hogy az ondansetronnal és dexametazonnal adott egyszeri adagú foszaprepitant (150 mg) nem volt kisebb a szokásos 3 napos orális aprepitant adagolásnál a CINV megelőzésében [96]. A fozaprepitantot poliszorbát 80-mal készítik, szolubilizáló szer, amely ritka, de súlyos túlérzékenységi reakciókat okozhat [97,98]
Netupitant
A Netupitant az NK-1 receptor kompetitív antagonistája, amelyet 300 mg netupitant és 0,5 mg palonosetront tartalmazó orális fix kombinációs termékként forgalmaznak. A kemoterápia előtt dexametazonnal együtt kapható akut és késleltetett CINV megelőzésére. Ezt a gyógyszerkombinációt sikeresen alkalmazták a magas és mérsékelten emetogén kemoterápiás beavatkozások megelőzésére [99,100]
Rolapitant
kortikoszteroidok
A szteroidokat általában más antiemetikumokkal együtt alkalmazzák. Antiemetikus hatásuk mechanizmusa nem teljesen ismert, de befolyásolhatják a prosztaglandin aktivitását az agyban. Klinikailag a szteroidok kvantitatív módon csökkentik vagy megszüntetik az NV epizódokat, és javíthatják a betegek hangulatát, ezáltal szubjektív jó közérzetet vagy eufóriát okozhatnak (bár depressziót és szorongást is okozhatnak). A szteroidokat néha egyszer használják az enyhén vagy mérsékelten emetogén kemoterápiában, de gyakrabban használják antiemetikus gyógyszerkombinációkban. [104,105] [A bizonyítékok szintje: I] [106]
A szteroidokat gyakran adják be orálisan vagy intravénásan a kemoterápia előtt, és megismételhetők. A dózisokat és az adagolási rendeket empirikusan választják ki. A dexametazon gyakran kezeli a NV választását az agyban sugárzásban részesülő betegeknél, mivel ez csökkenti az agyi ödémát is. Orálisan vagy intravénásan adják be a 8 mg és 40 mg közötti dózistartományban (gyermekkori dózis: 0,25-0,5 mg / kg). [107,108] A metilprednizolont orálisan vagy IV-ben adják be dózisokban és ütemezésekben, amelyek 40 mg-tól 500-ig terjednek mg 6-12 óránként legfeljebb 20 adagban [105,109]
A dexametazont szájon át is alkalmazzák a késleltetett NV esetében. A hosszú távú kortikoszteroid alkalmazása azonban nem megfelelő, és jelentős megbetegedést okozhat, beleértve a következőket: [110-112]
- Immunszuppresszió.
- Proximális izomgyengeség (különösen a combok és a felkarok bevonásával).
- A hosszú csontok aszeptikus nekrózisa.
- Szürkehályogképződés.
- Hyperglykaemia és a preexisting cukorbetegség súlyosbodása vagy a szubklinikai diabétesz klinikai patológiás expanziója.
- Adrenalin-szuppresszió hipokortiszolizmussal.
- Letargia.
- Hízás.
- GI-irritáció.
- Álmatlanság.
- Szorongás.
- A hangulat megváltozik.
- Pszichózis.
A petefészekrákos betegek csoportjában kemoterápiát vizsgáló vizsgálat azt találta, hogy a glükokortikoidok antiemetikumként történő rövid távú alkalmazása nem gyakorol negatív hatást az eredményekre (például a túlélés vagy a kemoterápia hatékonysága) [113]. Amint azt a metoklopramiddal korábban bemutattuk, számos tanulmány kimutatta, hogy a dexametazon fokozza az 5-HT antiemetikus tulajdonságait3[110,114] Intravénásan adva, a dexametazon 10-15 perc alatt adható be, mivel a gyors beadás általános melegség, garatzugging vagy égő érzést, vagy akut átmeneti perineális és / vagy végbél fájdalmat okozhat [115-118]
A benzodiazepinek
A benzodiazepinek, mint a lorazepám és az alprazolam, értékes segédanyagként ismertté váltak a szorongás megelőzésében és kezelésében, valamint a kemoterápiában részt vevő megelőző NV tüneteihez, különösen a gyermekek számára rendkívül emetogén adagolással. [110-112] A benzodiazepinek nem mutattak be intronikus antiemetikumot tevékenység egyetlen hatóanyagként; ezért antiemetikus profilaxisban és kezelésben való helyük más antiemetikus szerekhez is illeszkedik [119]. A benzodiazepinek feltehetően magasabb CNS-szerkezetekre, az agytörzsre és a gerincvelőre hatnak, és szorongásos, nyugtató és anterográfiai amnéziás hatásokat okoznak. Ezenkívül a benzodiazepinek jelentősen csökkentik az EPS, különösen az akathisia súlyosságát, a dopaminerg receptor antagonista antiemetikumokkal összefüggésben.
A lorazepám káros hatásai közé tartoznak a szedáció, észlelési és látászavarok, anterográfiai amnézia, zavartság, ataxia és depressziós mentális élettartam. [121] [121] [A bizonyítékok szintje: I] [122,123] Az Alprazolam hatékonynak bizonyult metoklopramiddal és metilprednizolonnal kombinálva [19]
Egyéb farmakológiai hatóanyagok
A növény kender több mint 60 különböző kannabinoid típust tartalmaz, vagy fiziológiai aktivitással rendelkező összetevőket. A legnépszerűbb, és talán a leginkább pszichoaktív delta-9-tetrahidrokannabinol (delta-9-THC). [124] Két FDA jóváhagyott kender CINV termékek:
- Dronabinol (szintetikus delta-9-THC), a CINV megelőzésére, 5 mg / m 2 orálisan 1-3 órával a kemoterápia előtt, és kemoterápia után 2-4 órával, összesen legfeljebb 6 adag naponta.
- A Nabilone-t, a CINV-re, amely nem reagált más antiemetikumokra, 1-2 mg orálisan naponta kétszer.
Ami a CINV-t illeti, kender a termékek valószínűleg a kannabinoid-1 (CB-1) és a CB-2 receptorokat célozzák meg, amelyek a központi idegrendszerben találhatóak [125]. Egy másik termék, a Sativex, delta-9-THC és kannabidiol kombinációját tartalmazza, és bukkális spray; klinikai vizsgálat alatt van [126,127]
Az ebbe az osztályba sorolt anyagokkal kapcsolatos kutatások nagy részét az 1970-es és 1980-as évek végén végezték, és összehasonlították a nabilon, a dronabinol vagy a levonantradollal a dopamin receptor, például a proklorperazin (Compazine) és a metoklopramid (Reglan) 132] Ez a tanulmánycsoport azt bizonyította, hogy a kannabinoidok olyan hatásosak voltak a mérsékelten emetogén kemoterápiára, mint a dopaminerg antiemetikumok, vagy hatékonyabbak voltak a placebónál. [124] A mellékhatások eufóriát, szédülést, diszfóriát, hallucinációt és hipotenziót tartalmaztak [124]. A hatékonyság korábbi jelentései ellenére, legalább egy vizsgálatban a betegek nem jelentették szignifikánsan a nabilonokat a mellékhatások miatt. [128]
Összefoglalva, a kender és a cannabinoidok a mai antiemetikumban a CINV megelőzésére és kezelésére nem ismeretesek. A betegekkel kapcsolatos megbeszélések a felhasználásról tartalmazhatnak válaszokat a rendelkezésre álló szerekre vonatkozóan, az ismert mellékhatásokról kender, és a kockázatok értékelését a terápia előnyeivel szemben [135].
Lásd a Cannabis és a kannabinoidok PDQ-összefoglalóját a környező problémák szélesebb körű megismeréséhez kender használat.
Egy 576 rákos beteg fázisú, véletlen besorolásos, dózisfelvételen végzett vizsgálata 576 rákos beteg esetében 0,5 g, 1 g és 1,5 g gyömbér helyett placebót adott napi kétszeri adagolásban az akut hányinger megelőzésére (az 1. nap utáni posztemoterápiának) azok a betegek, akiknek a jelenlegi kemoterápiás rendszere által okozott émelygés (11 pontos skálán mérve) a normál profilaxis ellenére 5-HT3 receptor antagonista. A betegek minden kemoterápiás kezelés előtt 3 nappal kezdték el a gyömbér- vagy placebo kapszulákat, és 6 napig folytatták őket. Az átlagos hányinger esetében 0,5 g gyömbér szignifikánsan jobb volt a placebónál; Mind a 0,5 g, mind az 1 g a “legrosszabb émelygés” szempontjából szignifikánsan jobb volt a placebóhoz képest. A késleltetett NV hatásai nem voltak szignifikánsak. Ez a vizsgálat nem ellenőrizte a kemoterápiás rendszabályok emetogenitását. A nemkívánatos események ritkák és nem súlyosak [23].
Többnapos kemoterápia
A kemoterápiás dózisok többszörös szekvenciális napokon (multiday kemoterápiával) történő együttes alkalmazása egyedülálló kihívást jelent a CINV megelőzésére, mivel az első kemoterápiás adag után az émelygés lehet akut és késleltetett. Bár a multiday kemoterápiára nincs standard antiemetikus kezelés, egy kortikoszteroid és egy 5-HT3 antagonistát kell alkalmazni a magas és mérsékelten emetogén kemoterápia minden napján [2,7,136] A bizonyíték előnyös az NK-1 antagonistának a magas és mérsékelten emetogén multiday kemoterápiához való hozzáadására [2,7,136,137] Az antiemetikus gyógyszerek és azok ütemezését össze kell hangolni az egyes kemoterápiás szerek emetogén hatásával és azok szekvenciájával. Emellett a késleltetett émelygés hossza változik, és az utolsó napi kemoterápia emetogenitásától függ.
A dexametazont a többnapos kemoterápiás kezelés minden napján tervezik, és 2-3 nappal azután, hogy fennáll a késleltetett hányinger kockázata. További dexametazon nem szükséges, ha a kemoterápiás kezelés kortikoszteroidot tartalmaz. Nem ismert, hogy a napi 20 mg dexametazonnal adott 5 napos ciszplatin-kezelés további antiemetikumot eredményez-e, és toxikus lehet-e. [137,138] Ezért egy alternatív dexametazon-ütemterv (20 mg az 1. és 2. napon, majd 8 mg naponta kétszer a 6. és 7. napon és napi kétszer 4 mg-on a 8. napon), a CINV időzítése és a teljes szteroid dózis csökkentése érdekében, 5 napos ciszplatin kezelésben részesülő betegeken [13,137]
A standard antiemetikus profilaxis 5-HT-t tartalmaz3 antagonistát adtak be az első kemoterápiás dózis előtt a többnapos kemoterápiás kezelés minden napján [2,7,136,137] 5-HT3 antagonistát előnyben részesítik az osztály többi ágense között a többnapos kemoterápiában. A palonosetron egy 5-HT3 antagonista, amely hosszabb felezési idővel és magasabb receptor-kötő affinitással rendelkezik, mint az osztály többi tagja, és ezáltal ritkábban lehet adni. [81] Egy leendő, ellenőrizetlen vizsgálat kimutatta, hogy a palonosetron, mint egyetlen IV dózis 20 mg dexametazonnal két 3 napos kemoterápiás kezelés előtt 80% CR-t eredményezett (hányás, mentés nélkül). [139] A palonoszetront dexametazonnal is profilaxisként tanulmányozták egy 5 napos ciszplatin-alapú csírasejt-daganatok kezelésére [13]. Ha a palonosetron és a dexametazon az 1., 3. és 5. napon, a betegek 51, 51% -ánál nem tapasztaltak hányást az 1-5. Napon, és 83% -uk nem észlelt hányást a 6-9. Napon. Alternatív módszerek az 5-HT3 antagonista adagolást vizsgáltunk.
A Granisetron 7 napos folyamatos transzdermális tapaszt hasonlították össze a napi orális granisetronnal többnapos kemoterápiában részesülő betegeknél egy kettős-vak, III. Fázisú noninferioritási vizsgálatban [74]. A tapasz a betegek 60% -ában teljes kontrollt mutatott, míg az orális készítmény a betegek 65% -ában, nem-inferioritással jár.
Az NK-1 antagonista aprepitantot és IV-formuláját, a fosaprepitantot multiday kemoterápiával vizsgálták olyan adagolási menetrendben, amelyek eltérnek az FDA által jóváhagyott ütemtervektől. Egy nem-randomizált vizsgálatban az aprepitant, a granisetron és a dexametazon CINV profilaxis alkalmazását értékelték 3 és 5 napos magas és mérsékelten emetogén kemoterápiával [140]. Az aprepitant 125 mg szájon át adva az első kemoterápiás adag beadása előtt, majd 80 mg szájon át a kemoterápia minden napján és 2 következő napon (összesen 5-7 nap). A CR-t 57,9% -ban, a magas és mérsékelten emetogén kemoterápiában részesülő betegek 72,5% -ánál figyelték meg. Hasonlóképpen ígéretes eredményeket találtunk egy későbbi, egykaros vizsgálatban, amely egy 7 napos orális aprepitant kezelést figyelt meg dexametazon és egy 5-HT3 antagonista 5 napos ciszplatin-alapú kemoterápiára [141]
Véletlenszerű, kettős-vak, placebo-kontrollált, az aprepitant, az 5-HT3 antagonistát és dexametazonot alkalmaztak olyan betegeknél, akik 5 napos ciszplatin-alapú kemoterápiát kaptak a csírasejt tumorok számára [95]. A 3. napon a szájon át adott aprepitant 125 mg volt, majd a napi 80 mg-os orális aprepitant követte a 4-7. Napokon. Több beteg az aprepitantra jutott, mint a placebóval, 42% a 13% -kal szemben (P
Magas dózisú kemoterápia őssejt-transzplantációval
A hányás megelőzése nagy dózisú kemoterápiában, a teljes test-besugárzással vagy anélkül továbbra is a betegellátás egyik kihívást jelentő területe. [143] A jelenlegi iránymutatások elsősorban egynapos terápiákra vonatkoznak; Emellett a hányás megelőzése a kemoterápia vagy a sugárterápia több napján alkalmazott napi egynapos tapasztalatokon alapul, további vizsgálatokra van szükség a betegek tüneteinek szabályozására. [143] Ez azt eredményezte, hogy NK-1 antagonistákat adnak hozzá a szerotonin antagonista és a dexametazon adagolásához. [143-145] További bizonyítékok szükségesek az optimális kombinációk meghatározásához, mivel a CR arányok 30% -nál alacsonyabbak [145]. A tapasztalat elsősorban az aprepitanttal történt; az újabb NK-1 antagonisták további előnyökkel járhatnak.
Összességében ezek az antiemetikus kombinációk jól toleráltak, a legtöbb mellékhatás a dexametazon-komponenst is magában foglalja; Továbbá, míg a gyógyszerkölcsönhatások eredetileg aggodalomra adtak okot, nem tűnnek klinikailag szignifikánsnak [146]. Továbbá, a hányás sokkal nagyobb mértékben szabályozódik, mint a hányinger, amely számos beteg számára továbbra is kihívást jelent. [143,147] Végül egy randomizált III. Fázisú vizsgálat során tanulmányozták az aprepitant, a granisetron és a dexamethason alkalmazását a CINV megelőzésére többszörös myeloma betegek, akik magas dózisú melfalanot kaptak autológ őssejt-transzplantációval. Statisztikailag pozitív haszon a mellékhatások növekedése nélkül, azoknál a betegeknél volt megfigyelhető, akik a három gyógyszeres kezelést kapták [144].
Jelenlegi klinikai vizsgálatok
Használja fejlett klinikai vizsgálati keresésünket, hogy megtalálja az NCI által támogatott rák klinikai vizsgálatokat, amelyek jelenleg beiratkozó betegek. A keresés szűkíthető a vizsgálat helye, a kezelés típusa, a gyógyszer neve és egyéb kritériumok alapján. A klinikai vizsgálatokkal kapcsolatos általános információk is rendelkezésre állnak.
Irodalom
- García Gómez J, Pérez López ME, García Mata J és munkatársai: SEOM klinikai iránymutatás antiemetikus profilaxis kezelésére kemoterápiát kapó rákos betegeknél. Clin Transl Oncol 12 (11): 770-4, 2010. [PUBMED Abstract]
- Basch E, Prestrud AA, Hesketh PJ és munkatársai: Antiemetikumok: American Society of Clinical Oncology klinikai gyakorlat útmutató frissítés. J Clin Oncol 29 (31): 4189-98, 2011. [PUBMED Abstract]
- Dupuis LL, Boodhan S, Holdsworth M és munkatársai: Iránymutatás gyermekgyógyászati rákos betegek daganatellenes gyógyszerei által okozott heveny hányinger és hányás megelőzésére. Pediatr Blood Cancer 60 (7): 1073-82, 2013. [PUBMED Abstract]
- Dupuis LL, Robinson PD, Boodhan S és munkatársai: Útmutató a gyermekgyógyászati rákos betegek kemoterápiájából származó előzetes hányinger és hányás megelőzésére és kezelésére. Pediatr Blood Cancer 61 (8): 1506-12, 2014. [PUBMED Abstract]
- Hesketh PJ: A kemoterápia által kiváltott hányinger és hányás patobiológiájának megértése. Alapvető terápiás előrelépés. Oncology (Williston Park) 18 (10 Suppl 6): 9-14, 2004. [PUBMED Abstract]
- Rudd JA, Andrews PLR: A rákellenes terápiák által kiváltott akut, késleltetett és megelőző hányás mechanizmusai. In: Hesketh PJ, ed .: Hányinger és hányás kezelése a rák és a rák kezelésében. Sudbury, Mass: Jones és Bartlett Publishers, Inc., 2005, 15-66. Oldal.
- National Comprehensive Cancer Network: Az NCCN klinikai gyakorlat irányelvei az onkológiában: Antiemesis. Verzió 2.2016. Fort Washington, Pa: Országos Átfogó Rákellenes Hálózat, 2016.
- Kris MG, Hesketh PJ, Somerfield MR és munkatársai: American Society of Clinical Oncology: antiemetikum oncology: update 2006. J Clin Oncol 24 (18): 2932-47, 2006. [PUBMED Abstract]
- Navari RM: A kemoterápia által kiváltott hányinger és hányás pathogenesis alapú kezelése – két új szer. J Support Oncol 1 (2): 89-103, 2003 Jul-Aug. [PUBMED Abstract]
- Grunberg SM, Deuson RR, Mavros P. et al .: A kemoterápia által kiváltott hányinger és hányás gyakorisága a modern antiemetikumok után. Cancer 100 (10): 2261-8, 2004. [PUBMED Abstract]
- Fabi A, Barduagni M, Lauro S. et al .: késleltetett kemoterápia indukálta hányás, amelyet jól kezeltek az onkológiai klinikai gyakorlatban? Egy megfigyelő tanulmány. Support Care Cancer 11 (3): 156-61, 2003. [PUBMED Abstract]
- Colagiuri B, Roscoe JA, Morrow GR és munkatársai: Hogyan viszonyulnak a betegek várható élettartamához, az életminőséghez és a postchemoterápia-hányingerhez? Cancer 113 (3): 654-61, 2008. [PUBMED Abstract]
- Einhorn LH, Brames MJ, Dreicer R és munkatársai: palonosetron és dexametazon a kemoterápia által kiváltott hányinger és hányás megelőzésére több napos ciszplatin kemoterápiában részesülő betegeknél. Support Care Cancer 15 (11): 1293-300, 2007. [PUBMED Abstract]
- Navari RM: A kemoterápia által kiváltott hányinger és hányás frissített antiemetikus irányelveinek áttekintése. Community Oncology 4 (4 Suppl 1): 3-11., 2007.
- Lexicomp Online. Hudson, Ohio: Lexi-Comp, Inc., 2018. Online elérhető előfizetéssel. Legutóbb elérte 2018. március 2-án.
- Gez E, Brufman G, Kaufman B és munkatársai: metilprednizolon és klórpromazin rákos kemoterápiában részesülő betegeknél: prospektív nem randomizált vizsgálat. J Chemother 1 (2): 140-3, 1989. [PUBMED Abstract]
- ASHP terápiás iránymutatások az émelygés és hányás farmakológiai kezelésére felnőtt és gyermekgyógyászati betegeknél kemoterápia, sugárkezelés vagy műtét során. Am J Health Syst Pharm 56 (8): 729-64, 1999. [PUBMED Abstract]
- Hurley JD, Eshelman FN: Trimetohobenzamid HCI a daganatellenes kemoterápiával kapcsolatos hányinger és hányás kezelésében. J Clin Pharmacol 20 (5-6 Pt 1): 352-6, 1980 május-június. [PUBMED Abstract]
- Mori K, Saito Y, Tominaga K: Az alprazolam antiemetikus hatásossága metoklopramid és metilprednizolon kombinációjában. Kettős vak véletlenszerű crossover vizsgálat ciszplatinnal indukált hányás esetén. Am J Clin Oncol 16 (4): 338-41, 1993. [PUBMED Abstract]
- Navari RM, Qin R, Ruddy KJ és munkatársai: olanzapin a kemoterápia által kiváltott hányinger és hányás megelőzésére. N Engl J Med 375 (2): 134-42, 2016. [PUBMED Abstract]
- Navari RM, Nagy CK, Gray SE: Olanzapin és metoklopramid alkalmazása emelkedett kemoterápiában részesülő betegekben áttörő kemoterápia által kiváltott hányinger és hányás kezelésére. Support Care Cancer 21 (6): 1655-63, 2013. [PUBMED Abstract]
- Todaro B: A kannabinoidok a kemoterápia által kiváltott hányinger és hányás kezelésében. J Natl Compr Canc Netw 10 (4): 487-92, 2012. [PUBMED Abstract]
- Ryan JL, Heckler CE, Roscoe JA és munkatársai: A gyömbér (Zingiber officinale) csökkenti az akut kemoterápia által kiváltott hányingert: 576 beteg URCC CCOP vizsgálata. Support Care Cancer 20 (7): 1479-89, 2012. [PUBMED Abstract]
- Marx WM, Teleni L, McCarthy AL és munkatársai: Ginger (Zingiber officinale) és kemoterápia által kiváltott hányinger és hányás: szisztematikus irodalmi áttekintés. Nutr Rev 71 (4): 245-54, 2013. [PUBMED Abstract]
- Olver IN, Webster LK, JF püspök és munkatársai: A proklorperazin adagolásának vizsgálata antiemetikumként a rák kemoterápiájához. Eur J Cancer Clin Oncol 25 (10): 1457-61, 1989. [PUBMED Abstract]
- Carr BI, Bertrand M, Browning S. és munkatársai: A proklorperazin és a metoklopramid antiemetikum hatékonyságának összehasonlítása a ciszplatin indukálta hányás kezelésére: prospektív, randomizált, kettős-vak vizsgálat. J Clin Oncol 3 (8): 1127-32, 1985. [PUBMED Abstract]
- Olver IN, Wolf M., Laidlaw C és munkatársai: A nagy dózisú intravénás proklorperazin randomizált, kettős vak vizsgálata, szemben a dózisos dózisú metoklopramid antiemetikumokkal a rák kemoterápiájára. Eur J Cancer 28A (11): 1798-802, 1992. [PUBMED Abstract]
- Levinson DF, Simpson GM: Neuroleptikus indukálta extrapiramidális tünetek lázzal. A “neuroleptikus malignus szindróma” heterogenitása. Psychiatry Arch. 43 (9): 839-48, 1986. [PUBMED Abstract]
- Wampler G: A fenotiazinok és a kapcsolódó gyógyszerek farmakológiai és klinikai hatékonysága a kemoterápia által kiváltott hányás kezelésére. Drugs 25 (Suppl 1): 35-51, 1983. [PUBMED Abstract]
- American Geriatrics Society 2012 Sörök kritériumainak frissítése Szakértői panel: Az American Geriatrics Society frissítette a söröket Az idősebb felnőtteknél a potenciálisan nem megfelelő gyógyszeres kezelés feltételei. J Am Geriatr Soc 60 (4): 616-31, 2012. [PUBMED Abstract]
- Mason BA, Dambra J, Grossman B és munkatársai: A ciszplatin által kiváltott hányinger hatékony ellenőrzése nagy dózisú szteroidok és droperidol alkalmazásával. Cancer Treat Rep 66 (2): 243-5, 1982. [PUBMED Abstract]
- Kelley SL, Braun TJ, Meyer TJ és munkatársai: A droperidol ciszplatin kemoterápia antiemetikumának vizsgálata. Cancer Treat Rep 70 (4): 469-72, 1986. [PUBMED Abstract]
- Plotkin DA, Plotkin D, Okun R: Haloperidol a hányinger és a hányás kezelésében citotoxikus gyógyszeradagolás miatt. Curr Ther Res Clin Exp 15 (9): 599-602, 1973. [PUBMED Abstract]
- Hardy JR, O’Shea A, White C és munkatársai: A haloperidol hatásossága hányinger és hányás kezelésében rákos betegeknél. J Pain Symptom Manage 40 (1): 111-6, 2010. [PUBMED Abstract]
- Bymaster FP, Falcone JF, Bauzon D és munkatársai: 5-HT (3) és 5-HT (6) receptorok hatásos antagonizálása olanzapinnal. Eur J Pharmacol 430 (2-3): 341-9, 2001. [PUBMED Abstract]
- ZYPREXA (olanzapin): a felírási információk legfontosabb elemei. Indianapolis, Ind: Eli Lilly és Company, 2018. Online elérhető. Utoljára 2018. március 1-jén érkezett.
- CM hocking, Kichenadasse G: Olanzapin kemoterápia által kiváltott hányinger és hányás esetén: szisztematikus felülvizsgálat. Support Care Cancer 22 (4): 1143-51, 2014. [PUBMED Abstract]
- Passik SD, Lundberg J, Kirsh KL és munkatársai: olanzapin antiemetikus aktivitásának kísérleti feltárása hányinger enyhítésére fejlett rákos megbetegedésben és fájdalomban szenvedő betegeknél. J Pain Symptom Manage 23 (6): 526-32, 2002. [PUBMED Abstract]
- Navari RM, Einhorn LH, Passik SD és munkatársai: olanzapin II. Fázisú kísérlete a kemoterápia által kiváltott hányinger és hányás megelőzésére: egy Hoosier Oncology Group tanulmány. Support Care Cancer 13 (7): 529-34, 2005. [PUBMED Abstract]
- Navari RM, Einhorn LH, Loehrer PJ Sr és munkatársai: olanzapin, dexametazon és palonosetron fázis II vizsgálata kemoterápia által kiváltott hányinger és hányás megelőzésére: Hoosier onkológiai csoportos vizsgálat. Support Care Cancer 15 (11): 1285-91, 2007. [PUBMED Abstract]
- Tan L, Liu J, Liu X és munkatársai: Olanzapin klinikai vizsgálata kemoterápia által kiváltott hányinger és hányás megelőzésére. J Exp Clin Cancer Res 28: 131, 2009. [PUBMED Abstract]
- Navari RM, Gray SE, Kerr AC: olanzapin és aprepitant a kemoterápia által kiváltott hányinger és hányás megelőzésére: véletlenszerű III. Fázisú vizsgálat. J Support Oncol 9 (5): 188-95, 2011 szept.-okt. [PUBMED Abstract]
- Mizukami N, Yamauchi M, Koike K és munkatársai: Olanzapin kemoterápia által kiváltott hányinger és hányás megelőzésére, magas vagy mérsékelten emetogén kemoterápiában részesülő betegeknél: randomizált, kettős-vak, placebo-kontrollos vizsgálatban. J Pain Symptom Manage 47 (3): 542-50, 2014. [PUBMED Abstract]
- Navari RM: Időszakos versus folyamatos infúzió metoklopramid összehasonlítása ciszplatin kemoterápia által kiváltott akut hányinger szabályozásában. J Clin Oncol 7 (7): 943-6, 1989. [PUBMED Abstract]
- Agostinucci WA, Gannon RH, Golub GR és munkatársai: Continuous i.v. infúzió és a metoklopramid többszörös bolusz dózisa a ciszplatin indukálta hányás megelőzésére. Clin Pharm 7 (6): 454-7, 1988. [PUBMED Abstract]
- Kris MG, Gralla RJ, Tyson LB és munkatársai: A ciszplatin indukálta emesis jobb kontrollja nagy dózisú metoklopramiddal és metoklopramid, dexametazon és difenhidramin kombinációival. 255 betegen végzett egymást követő vizsgálatok eredményei. Cancer 55 (3): 527-34, 1985. [PUBMED Abstract]
- Kris MG, Tyson LB, Gralla RJ és munkatársai: Extrapiramidális reakciók nagy dózisú metoklopramiddal. N Engl J Med 309 (7): 433-4, 1983. [PUBMED Abstract]
- Hsu ES: A granisetron, az 5-hidroxi-triptamin3 receptor antagonisták és más antiemetikumok áttekintése. Am J Ther 17 (5): 476-86, 2010 szept.-okt. [PUBMED Abstract]
- Trammel M, Roederer M, Patel J és munkatársai: A farmakogenomikát az akut kemoterápia által kiváltott hányinger és hányás szabályozása befolyásolja az 5-hidroxi-triptamin típusú 3-as receptor antagonistákkal szemben? Curr Oncol Rep 15 (3): 276-85, 2013. [PUBMED Abstract]
- Hatoum HT, Lin SJ, Buchner D és munkatársai: Különböző 5-HT3 RA antiemetikus rendellenességek összehasonlító klinikai hatékonysága a kemoterápia által kiváltott hányinger és hányás vonatkozásában a kórházi és sürgősségi osztály látogatásaihoz a valós világ gyakorlatában. Support Care Cancer 20 (5): 941-9, 2012. [PUBMED Abstract]
- Aogi K, Sakai H, Yoshizawa H és munkatársai: III. Fázisú nyílt vizsgálat a palonosetron biztonságosságának és hatásosságának a kemoterápia által kiváltott hányinger és hányás megelőzésére (CINV) emetogén kemoterápiában. Support Care Cancer 20 (7): 1507-14, 2012. [PUBMED Abstract]
- Hesketh PJ: Az 5-HT3 receptor antagonisták összehasonlító vizsgálata akut kemoterápia által kiváltott hányinger és hányás kezelésében. Cancer Invest 18 (2): 163-73, 2000. [PUBMED Abstract]
- Navari R, Gandara D, Hesketh P és munkatársai: Granisetron és ondansetron összehasonlító klinikai vizsgálata a ciszplatin indukálta hányás megelőzésében. A Granisetron tanulmányozócsoport. J Clin Oncol 13 (5): 1242-8, 1995. [PUBMED Abstract]
- Eisenberg P, Figueroa-Vadillo J, Zamora R és munkatársai: mérsékelten emetogén kemoterápia által kiváltott hányinger és hányás megelőzése palonoszetronnal, farmakológiailag új 5-HT3 receptor antagonistával: egy III. Fázisú, egyszeri dózisú vizsgálat vs. dolasetron . Cancer 98 (11): 2473-82, 2003. [PUBMED Abstract]
- Gralla R, Lichinitser M, Van Der Vegt S és munkatársai: a palonosetron javítja a kemoterápia által kiváltott hányinger és hányás megelőzését mérsékelten emetogén kemoterápia után: egy dupla vak randomizált III. Fázisú vizsgálat eredményei összehasonlítják a palonosetron és az ondanszetron egyszeri dózisát. Ann Oncol 14 (10): 1570-7, 2003. [PUBMED Abstract]
- Boccia R, Grunberg S, Franco-Gonzales E és munkatársai: Orális palonosetron hatásossága az intravénás palonosetronhoz képest a kemoterápia által kiváltott hányinger és hányás megelőzésére, közepesen emetogén kemoterápiához társítva. Support Care Cancer 21 (5): 1453-60, 2013. [PUBMED Abstract]
- Hickok JT, Roscoe JA, Morrow GR és munkatársai: 5-hidroxitriptamin-receptor antagonisták proklorperazinnal a doxorubicin által okozott késleltetett hányinger szabályozására: URCC CCOP randomizált kontrollos vizsgálat. Lancet Oncol 6 (10): 765-72, 2005. [PUBMED Abstract]
- Kris MG: Miért van szükségünk egy másik antiemetikumra? Csak kérdezz. J Clin Oncol 21 (22): 4077-80, 2003. [PUBMED Abstract]
- Tyers MB: Az ondansetron farmakológiai és preklinikai antiemetikus tulajdonságai. Semin Oncol 19 (4 Suppl 10): 1-8, 1992. [PUBMED Abstract]
- Kaasa S, Kvaløy S, Dicato MA és munkatársai: ondansetron és metoklopramid összehasonlítása kemoterápia által kiváltott hányinger és hányás megelőzésében: randomizált, kettős-vak vizsgálat. Nemzetközi Emesis Tanulmányi Csoport. Eur J Cancer 26 (3): 311-4, 1990. [PUBMED Abstract]
- Hainsworth J, Harvey W, Pendergrass K és munkatársai: az intravénás ondansetron, egy szelektív szerotonin antagonista, az intravénás metoklopramid vakcina összehasonlítása a nagy dózisú ciszplatin kemoterápiával kapcsolatos hányinger és hányás megelőzésében. J Clin Oncol 9 (5): 721-8, 1991. [PUBMED Abstract]
- De Mulder PH, Seynaeve C, Vermorken JB és munkatársai: Ondansetron a nagy dózisú metoklopramiddal összehasonlítva az akut és késleltetett ciszplatinnal kiváltott hányinger és hányás megelőzésében. Egy multicentrikus, randomizált, kettős-vak, crossover vizsgálat. Ann Intern Med 113 (11): 834-40, 1990. [PUBMED Abstract]
- Marty M, Pouillart P, Scholl S és munkatársai: az ondansetron (GR 38032F) 5-hidroxi-triptamin3 (szerotonin) -antagonistának összehasonlítása nagy dózisú metoklopramiddal a ciszplatin indukálta hányás szabályozásában. N Engl J Med 322 (12): 816-21, 1990. [PUBMED Abstract]
- Hesketh PJ: Az ondansetron versus metoklopramid összehasonlító vizsgálata akut ciszplatin indukálta hányás megelőzésében. Semin Oncol 19 (4 Suppl 10): 33-40, 1992. [PUBMED Abstract]
- Pectasides D, Mylonakis A, Varthalitis J és munkatársai: az ondansetron és a dexametazon két különböző dózisának összehasonlítása a ciszplatin indukálta hányás megelőzésében. Oncology 54 (1): 1-6, 1997 Jan-Feb. [PUBMED Abstract]
- Hasler SB, Hirt A, Ridolfi Luethy A és munkatársai: Ondansetron terhelési dózisok biztonsága rákos gyermekeknél. Support Care Cancer 16 (5): 469-75, 2008. [PUBMED Abstract]
- Amerikai Élelmiszer- és Gyógyszeradminisztráció: FDA Drug Safety Communication: Az ondansetronnal (Zofran) kapcsolatos QT-megnyúlás új információi. Silver Spring, Md: US Food and Drug Administration, 2012. Online elérhető. Utoljára 2018. március 9-én érkezett.
- Beck TM, Hesketh PJ, Madajewicz S és munkatársai: az intravénás ondansetron rétegzett, randomizált, kettős-vak összehasonlítása több dózisú dózisú adagolással szemben, két egyszeri adagolási rendben a ciszplatin által kiváltott hányinger és hányás megelőzésében. J Clin Oncol 10 (12): 1969-75, 1992. [PUBMED Abstract]
- Finn AL: Az ondansetron toxicitása és mellékhatásai. Semin Oncol 19 (4 Suppl 10): 53-60, 1992. [PUBMED Abstract]
- Coates AS, Childs A, Cox K és munkatársai: súlyos vascularis mellékhatások thrombocytopénia és veseelégtelenség emetogén kemoterápia és ondansetron után. Ann Oncol 3 (9): 719-22, 1992. [PUBMED Abstract]
- Ruff P, Paska W, Goedhals L és munkatársai: Ondansetron a graniszteronnal összehasonlítva a ciszplatin által kiváltott akut hányás megelőzésében: multicentrikus, kettős vak, randomizált, párhuzamos csoportos vizsgálat. Az Ondansetron és a Granisetron Emesis Study Group. Oncology 51 (1): 113-8, 1994 Jan-Feb. [PUBMED Abstract]
- Jantunen IT, Muhonen TT, Kataja VV és mtsai .: 5-HT3 receptor antagonisták a mérsékelten emetogén kemoterápia által kiváltott akut hányás megelőzésében – randomizált vizsgálat. Eur J Cancer 29A (12): 1669-72, 1993. [PUBMED Abstract]
- Gebbia V, Cannata G, Testa A és munkatársai: Ondansetron vs. granisetron a kemoterápia által kiváltott hányinger és hányás megelőzésében. Egy prospektív randomizált vizsgálat eredményei. Cancer 74 (7): 1945-52, 1994. [PUBMED Abstract]
- Boccia RV, Gordan LN, Clark G és munkatársai: A transzdermális granisetron hatásossága és tolerálhatósága a kemoterápia által kiváltott hányinger és hányás szabályozására, melyet mérsékelten és nagymértékben emetogén többnapos kemoterápiával társítanak: egy randomizált, kettős-vak, III. Fázisú vizsgálatot . Support Care Cancer 19 (10): 1609-17, 2011. [PUBMED Abstract]
- Amerikai Élelmiszer- és Gyógyszerbiztonsági Hatóság: FDA Drug Safety Communication: Az Anzemet (dolasetron mezilát) alkalmazásával járó rendellenes szívritmuszavarok. Silver Spring, Md: US Food and Drug Administration, 2010. Online elérhető. Utoljára 2018. március 9-én érkezett.
- Fauser AA, Duclos B, Chemaissani A és munkatársai: A dolasetron mezilát egyszeri dózisának és az ondansetron többszörös dózisának terápiás egyenértékűsége mérsékelt emetogén kemoterápia után hányás megelőzésére. Európai Dolasetron összehasonlító tanulmányozócsoport. Eur J Cancer 32A (9): 1523-9, 1996. [PUBMED Abstract]
- Eisenberg P, MacKintosh FR, Ritch P és munkatársai: A palonosetron hatásossága, biztonságossága és farmakokinetikája magas emetogén ciszplatin-alapú kemoterápiában részesülő betegeknél: dózisfüggő klinikai vizsgálat. Ann Oncol 15 (2): 330-7, 2004. [PUBMED Abstract]
- Tricco AC, Soobiah C, Antony J és munkatársai: Sebészeten és kemoterápiában részesülő betegeken szerotonin (5-HT3) receptor antagonisták biztonsága: protokoll szisztematikus felülvizsgálat és hálózati metaanalízis céljából. Syst Rev 2: 46, 2013. [PUBMED Abstract]
- Faria C, Li X, Nagl N és munkatársai: Eredmények 5-HT3-RA terápiás kiválasztással kemoterápia által kiváltott hányinger és hányás esetén: retrospektív követelések analízise. Am Health Drug Benefits 7 (1): 50-8, 2014. [PUBMED Abstract]
- Schwartzberg L, Barbour SY, Morrow GR és munkatársai: A palonosetron és az ondansetron, a dolasetron és a granisetron III. Fázisú klinikai vizsgálatainak összevont elemzése a kemoterápia által kiváltott hányinger és hányás megelőzésére (CINV). Support Care Cancer 22 (2): 469-77, 2014. [PUBMED Abstract]
- Affronti ML, Bubalo J: Palonosetron a kemoterápia által kiváltott hányinger és hányás kezelésében többnapos kemoterápiában részesülő betegeknél. Cancer Manag Res 6: 329-37, 2014. [PUBMED Abstract]
- Navari RM: Palonosetron a kemoterápia által kiváltott hányinger és hányás megelőzésére: jóváhagyás és hatásosság. Cancer Manag Res 1: 167-76, 2009. [PUBMED Abstract]
- Aapro MS, Grunberg SM, Manikhas GM és munkatársai: A palonosetron III. Fázisú, kettős-vak, randomizált vizsgálata az ondansetronnal szemben a kemoterápia által kiváltott hányinger és hányás megelőzésében, erősen emetogén kemoterápia után. Ann Oncol 17 (9): 1441-9, 2006. [PUBMED Abstract]
- Navari RM: Palonosetron: második generációs 5-hidroxi-triptamin receptor antagonista. Future Oncol 2 (5): 591-602, 2006. [PUBMED Abstract]
- Humphreys S, Pellissier J, Jones A: Az aprepitant kezelés költséghatékonysága a kemoterápia által kiváltott hányinger és hányás megelőzésére emlőrákos betegeknél az Egyesült Királyságban. Cancer Manag Res 5: 215-24, 2013. [PUBMED Abstract]
- Warr DG, Street JC, Carides AD: Az émelygés és a hányás előrejelzésére alkalmas kockázati tényezők értékelése az aktuális védelmi antiemetikummal: az aprepitant 3. fázisú vizsgálatának elemzése az adriamycin-ciklofoszfamid-alapú kemoterápiában részesülő betegeknél. Support Care Cancer 19 (6): 807-13, 2011. [PUBMED Abstract]
- Hesketh PJ, Aapro M, Street JC és munkatársai: Hányinger és hányás előrejelző tényezők értékelése az aktuális, óvodás elleni antiemetikus kezeléssel: aprepitant két fázisú vizsgálatának vizsgálata ciszplatin alapú kemoterápiában részesülő betegeknél. Support Care Cancer 18 (9): 1171-7, 2010. [PUBMED Abstract]
- Hu W, Fang J, Nie J és munkatársai: Az aprepitant hozzáadása növeli a ciszplatin által indukált hányás elleni védelmet, ha egy hagyományos hányásellenes kezelés sikertelen. Cancer Chemother Pharmacol 73 (6): 1129-36, 2014. [PUBMED Abstract]
- Poli-Bigelli S, Rodrigues-Pereira J, Carides AD és munkatársai: A neurokinin 1 receptor antagonista aprepitantnak a standard antiemetikus terápiához való hozzáadása növeli a kemoterápia által kiváltott hányinger és hányás szabályozását. Egy randomizált, kettős-vak, placebo-kontrollos vizsgálat eredménye Latin-Amerikában. Cancer 97 (12): 3090-8, 2003. [PUBMED Abstract]
- Hesketh PJ, Grunberg SM, Gralla RJ és munkatársai: orális neurokinin-1 antagonista aprepitant a kemoterápia által kiváltott hányinger és hányás megelőzésére: multinacionális, randomizált, kettős vak, placebo-kontrollos vizsgálat nagy dózisú betegeknél ciszplatin – az Aprepitant Protocol 052 vizsgálati csoport. J Clin Oncol 21 (22): 4112-9, 2003. [PUBMED Abstract]
- Schmoll HJ, Aapro MS, Poli-Bigelli S és munkatársai: Aprepitant-kezelés összehasonlítása többnapos ondansetron-kezeléssel, mind dezametazonnal, antiemetikus hatékonysággal a nagy dózisú ciszplatin kezelés során. Ann Oncol 17 (6): 1000-6, 2006. [PUBMED Abstract]
- Warr DG, Hesketh PJ, Gralla RJ és munkatársai: Az aprepitant hatásossága és tolerálhatósága kemoterápia által kiváltott hányinger és hányás megelőzésére mellrákos betegeknél mérsékelten emetogén kemoterápia után. J Clin Oncol 23 (12): 2822-30, 2005. [PUBMED Abstract]
- Rapoport BL, Jordan K, Boice JA és munkatársai: Aprepitant a kemoterápia által kiváltott hányinger és hányás megelőzésére, amely a közepesen emetogén kemoterápiák és tumor típusok széles köréhez kapcsolódik: egy randomizált, kettős-vak vizsgálat. Support Care Cancer 18 (4): 423-31, 2010. [PUBMED Abstract]
- Aapro MS, Schmoll HJ, Jahn F és munkatársai: Az aprepitant hatásosságának áttekintése kemoterápia által kiváltott hányinger és hányás megelőzésére számos daganat típusban. Cancer Treat Rev 39 (1): 113-7, 2013. [PUBMED Abstract]
- Albany C, Brames MJ, Fausel C és munkatársai: randomizált, kettős-vak, placebo-kontrollos, fázis III keresztkötésű vizsgálat, amely az orális neurokinin-1 antagonista aprepitantot 5HT3 receptor antagonistával és dexametazonnal kombinálva, sejtdaganatok, amelyek 5 napos ciszplatin kombinációs kemoterápiás kezelést kaptak: egy hoosier onkológiai csoportos vizsgálatot. J Clin Oncol 30 (32): 3998-4003, 2012. [PUBMED Abstract]
- Grunberg S, Chua D, Maru A és munkatársai: Egyszeri adagú fosaprepitant a ciszplatin terápiához társuló kemoterápia által kiváltott hányinger és hányás megelőzésére: randomizált, kettős-vak vizsgálati protokoll – EASE. J Clin Oncol 29 (11): 1495-501, 2011. [PUBMED Abstract]
- EMEND (Fosaprepitant Dimeglumine) injekcióhoz, intravénás alkalmazáshoz. Kenilworth, NJ: Merck Co., Inc., 2017. Online elérhető. Utoljára 2018. március 9-én érkezett.
- Shelley WB, Talanin N, Shelley ED: Poliszorbát 80 túlérzékenység. Lancet 345 (8960): 1312-3, 1995. [PUBMED Abstract]
- Hesketh PJ, Rossi G, Rizzi G és munkatársai: A NEPA hatékonysága és biztonságossága, a netupitáns és a palonosetron orális kombinációja a kemoterápia által kiváltott hányinger és hányás megelőzésére, magas emetogén kemoterápia után: randomizált dózisfüggő pivotal vizsgálat. Ann Oncol 25 (7): 1340-6, 2014. [PUBMED Abstract]
- Aapro M, Rugo H, Rossi G és munkatársai: randomizált III. Fázisú vizsgálat, amely a NEPA, a netupitáns és a palonosetron rögzített dózisú kombinációjának hatékonyságát és biztonságosságát értékeli a kemoterápia által kiváltott hányinger és hányás megelőzésére, mérsékelten emetogén kemoterápiát követően. Ann Oncol 25 (7): 1328-33, 2014. [PUBMED Abstract]
- Schwartzberg LS, Modiano MR, Rapoport BL és munkatársai: A robbantó biztonságossága és hatékonysága a kemoterápia által kiváltott hányinger és hányás megelőzésére közepesen emetogén kemoterápia vagy antraciklin és ciklofoszfamid adagolás után rákos betegekben: randomizált, aktív kontrollált, kettős vak, 3. fázisú vizsgálat. Lancet Oncol 16 (9): 1071-8, 2015. [PUBMED Abstract]
- Rapoport BL, Chasen MR, Gridelli C és munkatársai: a rop-tánsnak a kemoterápia által kiváltott hányinger és hányás megelőzésére való alkalmazásának biztonságossága és hatékonysága a cisplatin alapú, rendkívül emetogén kemoterápiában rákos betegeknél: két randomizált, vak, 3. fázisú vizsgálatok. Lancet Oncol 16 (9): 1079-89, 2015. [PUBMED Abstract]
- VARUBI (Rolapitant) tabletták, orális alkalmazásra. Waltham, Mass: TESARO, Inc., 2017. Elérhető online. Utoljára 2018. március 9-én érkezett.
- JF püspök, Matthews JP, Wolf MM és munkatársai: A kemoterápiában részesülő betegeknél a dezamethason, a lorazepám és a proklórperazin randomizált vizsgálata hányás esetén. Eur J Cancer 28 (1): 47-50, 1992. [PUBMED Abstract]
- Chiara S, Campora E, L. Lionetto és munkatársai: metilprednizolon a CMF indukálta hányás szabályozására. Am J Clin Oncol 10 (3): 264-7, 1987. [PUBMED Abstract]
- Parry H, Martin K: Egyadagos i.v. dexametazon – a rákos kemoterápiában hatékony antiemetikus. Cancer Chemother Pharmacol 28 (3): 231-2, 1991. [PUBMED Abstract]
- Cassileth PA, Lusk EJ, Torri S és munkatársai: A nagy dózisú dezoxametazon indirekt terápiájában fellépő antiemetikus hatékonysága akut non-lymphocytás leukémiában. Ann Intern Med 100 (5): 701-2, 1984. [PUBMED Abstract]
- Aapro MS, Plezia PM, Alberts DS, és munkatársai: A nagy dózisú dezoxametazon antioxidáns hatása a nagy dózisú metoklopramid antioxidáns hatására kettős-vak átfedéssel. J Clin Oncol 2 (5): 466-71, 1984. [PUBMED Abstract]
- Schallier D, Van Belle S, De Greve J és munkatársai: metilprednizolon antiemetikus gyógyszerként. Véletlenszerű kettős vak vizsgálat. Cancer Chemother Pharmacol 14 (3): 235-7, 1985. [PUBMED Abstract]
- Kris MG, Gralla RJ, Clark RA és munkatársai: egymást követő dózisfelvételi vizsgálatok a lorazepámnak a metoklopramid és a dexametazon kombinációjához való hozzáadásával: javult a szubjektív hatékonyság a difenhidramin és a metoklopramid valamint a dexametazon kombinációjánál. Cancer Treat Rep 69 (11): 1257-62, 1985. [PUBMED Abstract]
- Greenberg DB, Surman OS, Clarke J és munkatársai: Alprazolam a fób hányingerhez és hányáshoz a rák kemoterápiájához. Cancer Treat Rep 71 (5): 549-50, 1987. [PUBMED Abstract]
- Hockenberry-Eaton M, Benner A: Hányinger és hányás minták gyermekekben: ápolási értékelés és beavatkozás. Oncol Nurs Forum 17 (4): 575-84, 1990 július-aug. [PUBMED Abstract]
- Münstedt K, Borces D, Bohlmann MK és munkatársai: Glucocorticoid alkalmazása antiemetikus terápiában: biztonságos? Cancer 101 (7): 1696-702, 2004. [PUBMED Abstract]
- Roila F, Tonato M, Cognetti F és munkatársai: Ciszplatin indukálta hányás megelőzése: egy dupla-vak multicentrikus randomizált crossover vizsgálat, amely az ondansetront és az ondansetront és a dexametazont hasonlította össze. J Clin Oncol 9 (4): 675-8, 1991. [PUBMED Abstract]
- Zaglama NE, Rosenblum SL, Sartiano GP és munkatársai: Egyszeri, nagy dózisú intravénás dexametazon antiemetikumként a rák kemoterápiájában. Oncology 43 (1): 27-32, 1986. [PUBMED Abstract]
- Klygis LM: Dexametazon által indukált perineális irritáció a fejsérülésben. Am J Emerg Med 10 (3): 268, 1992. [PUBMED Abstract]
- Többet a dexametazon által indukált perineális irritációról. N Engl J Med 314 (25): 1643-4, 1986. [PUBMED Abstract]
- Baharav E, Harpaz D, Mittelman M és munkatársai: Dexamethason-indukált perineális irritáció. N Engl J Med 314 (8): 515-6, 1986. [PUBMED Abstract]
- Triozzi PL, Goldstein D, J. Laszlo: A benzodiazepinek hozzájárulása a rákterápiához. Cancer Invest 6 (1): 103-11, 1988. [PUBMED Abstract]
- János Laszlo, Clark RA, Hanson DC és munkatársai: a lazazepám a ciszplatinnal kezelt rákos betegeknél: antiemetikus, amnéziás és szorongásoldó hatású gyógyszerek. J Clin Oncol 3 (6): 864-9, 1985. [PUBMED Abstract]
- JF püspök, Olver IN, Wolf MM és munkatársai: Lorazepam: randomizált, kettős-vak, keresztkötéses vizsgálat egy új antiemetikumról citotoxikus kemoterápiában és proklorperazinnal kezelt betegeknél. J Clin Oncol 2 (6): 691-5, 1984. [PUBMED Abstract]
- Henry DW, Burwinkle JW, Klutman NE: A lorazepám nyugtató és amnesztikus dózisának meghatározása gyermekeknél. Clin Pharm 10 (8): 625-9, 1991. [PUBMED Abstract]
- van Hoff J, Olszewski D: Lorazepám gyermekek kemoterápiával kapcsolatos hányingerének és hányásának szabályozására. J Pediatr 113 (1 Pt 1): 146-9, 1988. [PUBMED Abstract]
- Ben Amar M: A kannabinoidok az orvostudományban: Terápiás potenciáljuk felülvizsgálata. J Ethnopharmacol 105 (1-2): 1-25, 2006. [PUBMED Abstract]
- Davis MP: Orális nabilone kapszulák kemoterápia által kiváltott hányinger és hányás kezelésére. Expert Opin Investig Drugs 17 (1): 85-95, 2008. [PUBMED Abstract]
- Duran M, Pérez E, Abanades S és munkatársai: A kemoterápia által kiváltott hányinger és hányás előtti hatékonysága és biztonságossága oromucosalis standardizált kannabiszkivonat. Br J Clin Pharmacol 70 (5): 656-63, 2010. [PUBMED Abstract]
- Machado Rocha FC, Stéfano SC, De Cássia Haiek R és munkatársai: Cannabis sativa terápiás alkalmazása kemoterápia által kiváltott hányinger és hányás között rákos betegek körében: szisztematikus felülvizsgálat és metaanalízis. Eur J Cancer Care (Engl) 17 (5): 431-43, 2008. [PUBMED Abstract]
- Ahmedzai S, Carlyle DL, Calder IT és munkatársai: nabilon, szintetikus kannabinoid, a tüdőrák kemoterápiájában alkalmazott antiemetikus hatékonyság és toxicitás. Br J Cancer 48 (5): 657-63, 1983. [PUBMED Abstract]
- Chan HS, Correia JA, MacLeod SM: Nabilone versus prochlorperazine a rák kemoterápiás indukálta hányás szabályozásában gyermekeknél: kettős-vak, crossover kísérlet. Pediatrics 79 (6): 946-52, 1987. [PUBMED Abstract]
- Johansson R, Kilkku P, Groenroos M: A daganatos kemoterápia által kiváltott refrakter hányás kettős-vak, kontrollos vizsgálata a nabilon vs. proklorperazin ellen. Cancer Treat Rev 9 (Suppl B): 25-33, 1982. [PUBMED Abstract]
- Niiranen A, Mattson K: A nabilon és a proklorperazin keresztmetszeti összehasonlítása a rák kemoterápia által indukált hányás miatt. Am J Clin Oncol 8 (4): 336-40, 1985. [PUBMED Abstract]
- Tramèr MR, Carroll D, Campbell FA és munkatársai: Kannabinoidok a kemoterápia által kiváltott hányinger és hányás szabályozására: kvantitatív szisztematikus felülvizsgálat. BMJ 323 (7303): 16-21, 2001. [PUBMED Abstract]
- Meiri E, Jhangiani H, Vredenburgh JJ és munkatársai: A dronabinol önmagában és ondansetron és csak ondansetron kombinációjának hatása késleltetett kemoterápia által kiváltott hányinger és hányás esetén. Curr Med Res Opin 23 (3): 533-43, 2007. [PUBMED Abstract]
- Strasser F, Luftner D, Possinger K és munkatársai: Orálisan beadott kannabiszkivonat és delta-9-tetrahidrocannabinol összehasonlítása rákkal kapcsolatos anorexia-cachexia szindrómában szenvedő betegek kezelésében: multicentrikus, fázis III, randomizált, kettős vak, placebo – kontrollált klinikai vizsgálat a Cannabis-In-Cachexia-Study-csoportból. J Clin Oncol 24 (21): 3394-400, 2006. [PUBMED Abstract]
- Coffman KL: A marihuána használatáról szóló vita a transzplantációs jelöltekben: a közelmúlt orvosi bizonyítékai a marihuána egészségügyi hatásairól. Curr Opin Organ Transplant 13 (2): 189-95, 2008. [PUBMED Abstract]
- Einhorn LH, B Rapoport, Koeller J és munkatársai: Többnapos kemoterápia és magas dózisú kemoterápia őssejt-transzplantációval végzett heurémiás kezelés: áttekintés és konszenzus megállapítás. Support Care Cancer 13 (2): 112-6, 2005. [PUBMED Abstract]
- Roila F, Herrstedt J, Aapro M és munkatársai: Útmutató frissítés a MASCC és az ESMO számára kemoterápia és radioterápia által kiváltott hányinger és hányás megelőzésében: a Perugia konszenzus konferencia eredményei. Ann Oncol 21 (Suppl 5): v232-43, 2010. [PUBMED Abstract]
- Baltzer L, Pisters KM, Kris MG és munkatársai: nagy dózisú ondansetron (OND) és dexametazon (DEX) a hányinger és a hányás megelőzésére több napos ciszplatin kemoterápiával. [Abstract] Az American Society of Clinical Oncology 12: A-1607, 462, 1993.
- Lorusso V, Giampaglia M, Petrucelli L és munkatársai: Egyszeri dózisú palonosetron és dexametazon antiemetikus hatásossága többnapos kemoterápiás többszörös ciklusú betegeknél. Support Care Cancer 20 (12): 3241-6, 2012. [PUBMED Abstract]
- Jordan K, Kinitz I., Voigt W és munkatársai: Hármas antiemetikus kombináció biztonságossága és hatékonysága az NK-1 antagonista aprepitanttal erősen és közepesen emetogén többnapos kemoterápiában. Eur J Cancer 45 (7): 1184-7, 2009. [PUBMED Abstract]
- Olver IN, Grimison P, Chatfield M és munkatársai: 7 napos aprepitant adagolási rend eredményei hányinger és hányás megelőzésére 5 napos ciszplatin alapú csírasejt tumor kemoterápiában. Support Care Cancer 21 (6): 1561-8, 2013. [PUBMED Abstract]
- Adra N, Albany C, Brames MJ és munkatársai: Foszaprepitant + 5HT3 receptor antagonista + dexametazon fázis II. Vizsgálata 5 napos ciszplatin alapú kemoterápiában részesülő csírasejtes tumoros betegeknél: Hoosier Cancer Research Network vizsgálat. Support Care Cancer 24 (7): 2837-42, 2016. [PUBMED Abstract]
- Stiff PJ, Fox-Geiman MP, Kiley K és munkatársai: Az őssejt-transzplantációval összefüggő hányinger és hányás megelőzése: az emelkedett emetogén preparatív kezelések során alkalmazott aprepitant prospektív, randomizált vizsgálata. Biol vérképző transzplantátum 19 (1): 49-55.e1, 2013. [PUBMED Abstract]
- Schmitt T, Goldschmidt H, Neben K és munkatársai: Aprepitant, granisetron és dexametazon a kemoterápia által kiváltott hányinger és hányás megelőzésére a nagy dózisú melfalán után autológ transzplantáció esetén multiple myeloma esetén: randomizált, placebo-kontrollos III. Fázis próba. J Clin Oncol 32 (30): 3413-20, 2014. [PUBMED Abstract]
- Sakurai M, Mori T, Kato J és munkatársai: Az aprepitant hatékonysága az émelygés és hányás megelőzésére nagy dózisú melphalan alapú kondicionálásnak köszönhetően allogén vérképző őssejt-transzplantációra. Int J Hematol 99 (4): 457-62, 2014. [PUBMED Abstract]
- Bubalo JS, Cherala G, McCune JS és munkatársai: Aprepitant farmakokinetikája és az aprepitant hatásának felmérése a ciklofoszfamid-anyagcserére a hematopoietikus őssejt-transzplantációban részesülő rákos betegeknél. J Clin Pharmacol 52 (4): 586-94, 2012. [PUBMED Abstract]
- Yeh SP, Lo WC, Hsieh CY és munkatársai: palonosetron és dexametazon a hányinger és a hányás megelőzésére allogén vérképző őssejt-transzplantációban részesülő betegeknél. Support Care Cancer 22 (5): 1199-206, 2014. [PUBMED Abstract]
Émelygés és hányás nem farmakológiai kezelésére (NV)
Nem farmakológiai stratégiákat alkalmaznak az NV kezelésére. Ezek a következők:
- Étrendi változások. (További információért lásd a táplálkozás a rák kezelésében című PDQ-összefoglalót.)
- Hipnózis.
- Akupunktúra. (További információ az Akupunktúra PDQ-összefoglalójában található.)
- Akupresszúra.
- Relaxációs technikák.
- Viselkedési terápia.
- Irányított képek.
Az előretekintő NV (ANV) leggyakrabban vizsgált kezelése az irányított képalkotás, a hipnózis és a progresszív izomlazítás eszközeként alkalmazott szisztematikus deszenzitizáció volt, és ez a klasszikusan kondicionált válasz javasolt kezelése. (További információkért olvassa el az összefoglaló ANV részének kezelését.)
Sugárzás által kiváltott hányinger és hányás (RINV)
Bevezetés
A radioterápia (RT) a rákos betegeknél a hányinger és hányás (NV) egyik fontos oka. A megfigyelési tanulmányok azt mutatják, hogy az RT egy bizonyos fokú NV-je 80% -os összesített előfordulási aránya [1]. Az NV kifejlesztésének kockázati tényezői ismertek. Az RINV rontja az életminőséget, ami a kezeléssel járó késedelmeket és a megbontott találkozókat eredményezi, ami rákkeltő hatású. [2,3]
Járványtan
Két nagy prospektív megfigyelési tanulmány ad tájékoztatást az RINV és az antiemetikus hatások gyakoriságáról. A radioterápia elleni antiemetikummal foglalkozó olasz csoport a RINV előfordulását 1020 különböző típusú sugárterápiában részesülő betegen vizsgálta [4]. Összességében a betegek 28% -ánál jelentették hányinger, hányás vagy mindkettőt. A hányás első epizódjának medián időtartama 3 nap volt. Antiemetikus gyógyszereket adtak be a betegek 17% -ánál, beleértve 12% -át profilaktikusan és 5% -os mentési terápiában. Egy 368, RT-t szedő betegen egy második csoportban a hányinger 39% -os, a hányás 7% -os volt. Hányinger gyakoribb volt azoknál, akik az alvosban vagy a medencében (66%) részesültek, mint a rákkeltő betegeknél a fej és a nyak területén (48%). Az antiemetikumok az RT alatt vannak feltüntetve. [6]
Kórélettani
Az RINV patofiziológiája nem teljesen ismert. A szerotonin, a P anyag és a dopamin neurotranszmitterek, amelyek a sugárzás által indukált hányásban vesznek részt. [7] Az RINV szoros hasonlóságot mutat a kemoterápiával indukált NV-vel (CINV). A szerotonin antagonisták hatékonysága az RINV-ben támogatja a szerotonin szerepét a sugárzás által indukált hányásban [7]. Az anyag P antagonistákat nem használják a RINV-ben olyan mértékben, mint amilyenek a CINV-ben. A preklinikai munka a P anyag szerepét mutatja a RINV-ban [8]. Az anyag P antagonistáit csak RINV-ra kezdték tanulmányozni. A P hatóanyag szerepet játszhat a hosszú távú NV-ben a RT adagolása után.
Kockázati rétegződés
A sugárterületi hely, a térfogat, a frakcionálási ütemterv és az egyszeri és teljes dózis meghatározza a RINV incidenciáját és súlyosságát. A legfontosabb tényező a sugárzás területén jelenik meg. A 4. táblázat a Rákkeltő Táplálék-ellátás Multinacionális Szövetsége (MASCC), az Európai Orvosi Onkológiai Társaság (ESMO) és az Amerikai Klinikai Onkológiai Társaság (ASCO) által javasolt kockázati kategóriákat mutatja be. Az osztályozás során nem veszik figyelembe az émelygés veszélyét. [10] Az RT kockázata, hogy egy beteg RT-vel kezelt, számos egyéb tényezőtől függ, az adott RT-rend rendszer emetogenitásán kívül. A betegspecifikus tényezők közé tartozik a kemoterápia, az életkor, a nem, az alkoholfogyasztás, a szorongás és az RINV vagy CINV korábbi tapasztalatainak egyidejű alkalmazása.
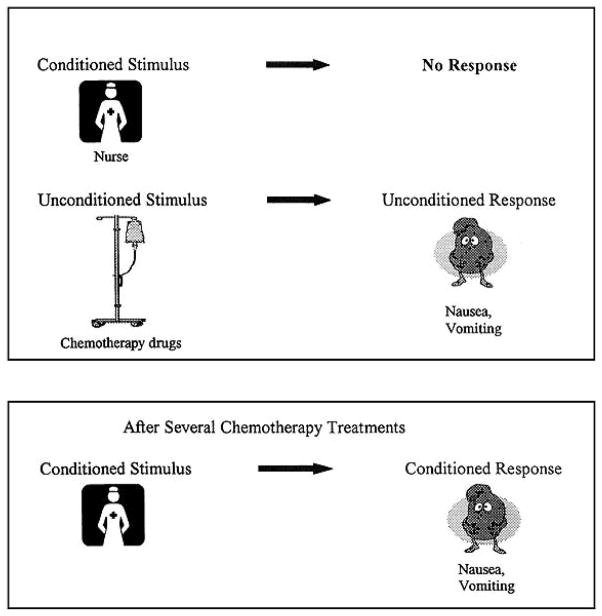
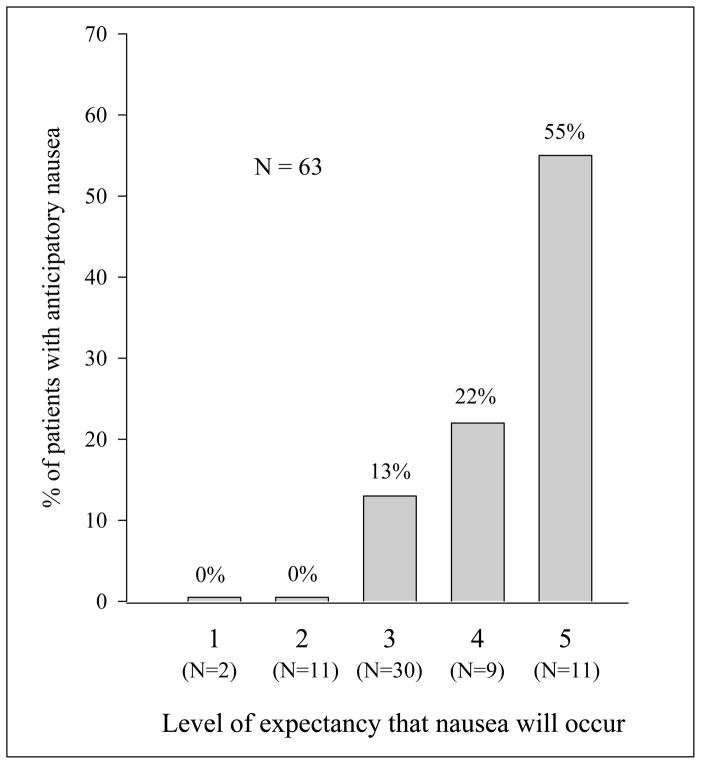


Kommentek
Kommenteléshez kérlek, jelentkezz be: