Vese-sejtes karcinóma kezelési rend
RENAL CELL CARCINOMA KEZELÉSI REGIMENS
Klinikai vizsgálatok: A National Comprehensive Cancer Network a rákos betegek részvételét ajánlja a klinikai vizsgálatokban, mint a kezelési arany standard.
A rák terápiás kiválasztása, adagolása, beadása és a kapcsolódó nemkívánatos események kezelése összetett folyamat lehet, amelyet egy tapasztalt egészségügyi szakembernek kell kezelnie. A klinikusoknak az egyes betegek alapján kell kiválasztaniuk és ellenőrizniük a kezelési lehetőségeket; a gyógyszeradag módosításokat és a támogató gondozási beavatkozásokat ennek megfelelően kell alkalmazni. Az alább felsorolt rákkezelési módok magukban foglalhatják mind az USA Food and Drug Administration jóváhagyott, mind a nem jóváhagyott indikációkat / kezeléseket. Ezek a kezelések csak a legújabb kezelési stratégiák kiegészítésére szolgálnak.
Ezek az iránymutatások olyan folyamatban lévő munkák, amelyeket olyan gyakran finomíthatnak, amilyen gyakran új, jelentős adatok állnak rendelkezésre. Az NCCN Guidelines® a szerzõk konszenzusos nyilatkozata a jelenleg elfogadott kezelési megközelítésekkel kapcsolatos nézeteikrõl. Bármelyik klinikus, aki az NCCN Guidelines® alkalmazására vagy konzultációjára törekszik, várhatóan önálló orvosi megítélést alkalmaz az egyedi klinikai körülmények összefüggésében a beteg ellátásának vagy kezelésének meghatározására. Az NCCN semmiféle garanciát nem vállal tartalmukra, felhasználásukra vagy alkalmazásukra vonatkozóan, és semmilyen felelősséget nem vállal az alkalmazásukért vagy bármilyen módon történő felhasználásért.
Általános kezelési megjegyzések: 1
• A tirozin-kináz inhibitorokat és az anti-érrendszeri endotéliás növekedési faktor antitesteket célzó terápiát széles körben alkalmazzák vese-sejtes karcinóma (RCC) első és második vonalbeli kezelésében. Eddig a hét ilyen hatóanyagot az FDA jóváhagyta a fejlett RCC kezelésére: sunitinib, sorafenib, pazopanib, axitinib, temsirolimus, everolimusz és bevacizumab és interferon kombinációi.
• A célzott terápiák megkezdése előtt a szisztémás kezelési lehetőségek a citokin terápiára korlátozódtak, nevezetesen az IL-2 és az interferon-α-2A (IFN-α-2a).
Első vonalbeli terápia túlnyomórészt tiszta sejtszövettel rendelkező betegek számára 1
Megjegyzés: Minden ajánlás 2A kategória, kivéve, ha másképpen jelezzük. A regényeket betűrendben, kategóriák és preferenciák szerint sorolják fel.
© 2018 Haymarket Media, Inc.
Pazopanib (1. kategória, előnyös) 2,3
Pazopanib 800 mg naponta egyszer orálisan étkezés nélkül.
Sunitinib (1. kategória, előnyös) 4,5
A Sunitinib 50 mg szájon át naponta étkezés közben vagy anélkül 4 hétig, majd 2 héttel később.
Bevacizumab + IFN-α (1. kategória) 6-8
Bevacizumab 10 mg / kg IV kéthetente + IFN-a.
Temsirolimus (1. kategória: rossz prognózisú betegek, 2B kategória: más kockázati csoportok kiválasztott betegei) 9,10
Temsirolimus 25 mg iv. 30-60 percenként hetente egyszer a betegség progressziójáig vagy elfogadhatatlan toxicitásig.
Az Axitinib 5 mg szájon át 12 óránként.
Cabozantinib (rossz és közepes kockázatú csoportok esetén) 13
Cabozantinib 60 mg naponta egyszer orálisan.
Magas dózisú IL-2 (kiemelkedő teljesítményű és normál orgonafunkciójú kiválasztott betegek esetében) 13,14, b
Az 1-5. És a 15-19. Napok: IL-2 600 000 NE / kg IV 8 óránként (legfeljebb 14 adag).
Ismételje meg a ciklust 4 hétente maximum 3 cikluson keresztül.
Utólagos terápia túlnyomórészt tiszta sejtkarcinóma esetén 1
Cabozantinib (1. kategória, előnyös) 16, d
A Cabozantinib 60 mg naponta egyszer, orálisan, táplálék nélkül, amíg a betegség progressziója vagy elfogadhatatlan toxicitás nem következik be.
Nivolumab (1. kategória, előnyös) 17,18, d
A Nivolumab 240 mg iv. Kéthetente a betegség progressziójáig vagy elfogadhatatlan toxicitásig.
Axitinib (1. kategória) 11,12, a
Az Axitinib 5 mg szájon át 12 óránként.
Lenvatinib + everolimusz (1. kategória) 19
A Lenvatinib 18 mg orálisan naponta egyszer + everolimusz 5 mg orálisan naponta egyszer, étellel vagy anélkül, amíg a betegség progressziója vagy elfogadhatatlan toxicitás nem áll fenn.
Everolimus 10 mg szájon át naponta egyszer étellel vagy anélkül.
Pazopanib 800 mg naponta egyszer orálisan étkezés nélkül.
Sorafenib 400 mg orálisan napi kétszer étkezés nélkül.
A Sunitinib 50 mg szájon át naponta étkezés közben vagy anélkül 4 hétig, majd 2 héttel később.
Bevacizumab (2B kategória) 28
Bevacizumab 10mg / kg IV kéthetente.
Magas dózisú IL-2 (kiváló teljesítményű és normál szervfunkciójú betegek esetében) (2B kategória) 14,15, b
Az 1-5. És a 15-19. Napok: IL-2 600 000 NE / kg IV 8 óránként (legfeljebb 14 adag).
Ismételje meg a ciklust 4 hétente maximum 3 cikluson keresztül.
Temsirolimusz (2B kategória) 31,32
Temsirolimusz 25 mg iv. 30-60 percenként hetente a betegség progressziójáig vagy elfogadhatatlan toxicitásig.
Szisztémás terápia nem tisztított sejtek szövettani betegeivel 1
Sunitinib (előnyös) 4,26,27
A Sunitinib 50 mg szájon át naponta étkezés közben vagy anélkül 4 hétig, majd 2 héttel később.
Az Axitinib 5 mg szájon át 12 óránként.
Bevacizumab 10mg / kg IV kéthetente.
Bevacizumab + erlotinib (a fejlett papilláris RCC-t tartalmazó HLRCC esetében) 29, f
1. nap: Bevacizumab 10 mg / kg IV
1-14. Nap: Az erlotinib 150 mg naponta egyszer orálisan.
Ismételje meg a ciklust 14 naponként.
Bevacizumab + everolimusz (a fejlett papilláris RCC-t tartalmazó HLRCC esetében) 30, f
1. nap: Bevacizumab 10 mg / kg IV
1-14. Nap: Everolimus 10 mg naponta egyszer orálisan.
Ismételje meg a ciklust 14 naponként.
A Cabozantinib 60 mg naponta egyszer, orálisan, táplálék nélkül, amíg a betegség progressziója vagy elfogadhatatlan toxicitás nem következik be.
Erlotinib 150 mg naponta egyszer orálisan étkezés nélkül.
Everolimus 10 mg szájon át naponta egyszer étellel vagy anélkül.
Lenvatinib + everolimus 19
A Lenvatinib 18 mg orálisan naponta egyszer + everolimusz 5 mg orálisan naponta egyszer, étellel vagy anélkül, amíg a betegség progressziója vagy elfogadhatatlan toxicitás nem áll fenn.
A Nivolumab 240 mg iv. Kéthetente a betegség progressziójáig vagy elfogadhatatlan toxicitásig.
Pazopanib 800 mg naponta egyszer orálisan étkezés nélkül.
Sorafenib 400 mg orálisan napi kétszer étkezés nélkül.
Temsirolimus (1. kategória: rossz prognózisú betegek, 2A kategória: más kockázati csoportok kiválasztott betegei) 27,28
Temsirolimusz 25 mg iv. 30-60 percenként hetente a betegség progressziójáig vagy elfogadhatatlan toxicitásig.
a májusi növekedés 7 hónap után 12 órával 2 hét után, kritériumok alapján; 2 héttel 12 óránként 10 mg-ra emelkedhet a kritériumok alapján.
b Kezelések 60 napos tanfolyamokra osztva, minden egyes IV-es kezelési ciklusban, amely két ciklusú terápiából áll, és kb. 7-10 nap pihenőidővel elválasztva, a 60 nap hátralevő részében semmilyen más terápiával.
c A progresszív betegek dózisát 600 mg-ra növelték napi kétszer.
d A III. fázisú vizsgálatok eredményei alapján a feljogosított betegeknek előnyben kell részesíteniük ezt az ágenst az everolimusz felett.
Az erlotinibet RCC-nél használják. Az NCCN iránymutatásai közé tartozik az opcionális elsővonalbeli terápia a relapszusos vagy orvosi szempontból nem tapasztalt IV. Stádiumú, nem tisztított sejtes karcinómában szenvedő betegek számára.
f HLRCC: Örökletes leiomyomatosis és vesesejtes rák.
1. Az NCCN Clinical Practice Guidelines in Oncology ™ engedélyével hivatkozva. Vese. v 3.2018. Elérhető a következő címen: http://www.nccn.org/professionals/physician_gls/pdf/ kidney.pdf. 2018. február 20-án lépett be.
2. Votrient [csomag-betét]. Research Triangle Park, NC: GSK; 2016.
3. Sternberg CN, Davis ID, Mardiak J et al. Pazopanib lokálisan előrehaladott vagy metasztatikus vesesejtes karcinóma esetén: véletlenszerű III. Fázisú vizsgálat eredménye. J Clin Oncol. 2010-ben; 28: 1061-1068.
4. Sutent [csomag-betét]. New York, NY: Pfizer Labs; 2016.
5. Gore ME, Szczylik C, Porta C et al. A szunitinib biztonságossága és hatékonysága metasztatikus vese-sejtes karcinóma esetén: kiterjesztett hozzáférésű vizsgálat. Lancet Oncol. 2009, 10: 757-763.
6. Avastin [csomag-betét]. San Francisco, CA: Genentech; 2016.
7. Escudier B, Pluzanska A, Koralewski P. et al; AVOREN Trialisták. Bevacizumab és interferon alfa-2a metasztatikus vesesejtes karcinóma kezelésére: randomizált, kettős-vak III. Fázisú vizsgálat. Lancet. 2007 370: 2103-2111.
8. Rini BI, Halabi S, Rosenberg JE et al. A bevacizumab és az interferon alfa interferon alfa monoterápia III. Szakaszában végzett vizsgálata metasztatikus vesesejtes karcinóma esetén: a CALGB 90206 végeredményei. J Clin Oncol. 2010-ben; 28: 2137-2143.
9. Torisel [csomag-betét]. Philadelphia, PA: Wyeth; 2016.
10. Hudes G, Carducci M, Tomczak P és munkatársai; Global ARCC Trial. Temsirolimus, interferon alfa vagy mindkettő a fejlett vesesejtes karcinóma esetén. N Engl J Med. 2007 356: 2271-2281.
11. Inlyta [csomag-betét]. New York, NY: Pfizer Inc.; 2016.
12. Rini BI, Escudier B, Tomczak P et al. Az axininib és a sorafenib összehasonlító hatékonysága a fejlett vesesejtes karcinómában (AXIS): randomizált fázisú 3-as vizsgálat. Lancet. 2011-ben; 378: 1931-1939.
13. Choueiri TK, Halabi S, Sanford BL, et al. Cabozantinib vs. szunitinib mint kezdeti célzott terápia szegény vagy közepes kockázatú metasztatikus vese-karcinómás betegek esetében: az Alliance A031203 CABOSUN próba. J Clin Oncol. 2017-re; 35: 591-597.
14. Proleukin [csomag-betét]. San Diego, CA: Prometheus Laboratories; 2016.
15. McDermott DF, Regan MM, Clark JI és mtsai. A nagy dózisú interleukin-2 szubkután interleukin és interferon randomizált fázis III vizsgálata metasztatikus vesesejtes karcinóma esetén. J Clin Oncol. 2005 23: 133-141.
16. Choueiri TK, Escudier B, Powles T és munkatársai; METEOR nyomozók. Cabozantinib versus everolimus a fejlett vese-sejt karcinómában. N Engl J Med. 2015-ig; 373 (19): 1814-1823.
17. Motzer RJ, Escudier B, McDermott DF és munkatársai; CheckMate 025 Investigators. Nivolumab versus everolimus a fejlett vese-sejt karcinóma. N Engl J Med. 2015-ig; 373 (19): 1803-1813.
18. Opdivo [csomag-betét]. Princeton, NJ: Bristol-Myers Squibb cég; 2016.
19. Lenvima [csomag-betét]. Woodcliff Lake, NJ: Eisai Inc.; 2016.
20. Afinitor [csomag-betét]. East Hanover, NJ: Novartis; 2016.
21. Motzer RJ, Escudier B, Oudard S és munkatársai; RECORD-1 tanulmányozócsoport. Az everolimusz hatásossága a fejlett vesesejtes karcinóma esetében: kettős vak, randomizált, placebo-kontrollos III. Fázisú vizsgálat. Lancet. 2008 372: 449-456.
22. Nexavar [csomag-betét]. Wayne, NJ: Bayer HealthCare; 2016.
23. Escudier B, Eisen T, Stadler WM, et al. Sorafenib a fejlett, egyértelmű vese-sejtes karcinóma sejtekben. N Engl J Med. 2007; 356: 125-134. Di Lorenzo G, Carteni G, Autorino R, et al. A szorafenib II. Fázisú vizsgálata szunitinib-refrakter metasztatikus vesesejtes rákos betegeknél. J Clin Oncol. 2009-ben; 27: 4469-4474.
25. Garcia JA, Hutson TE, Elson P. et al. Sorafenib olyan betegeknél, akik metasztatikus vese-karcinómában szisztémásan vagy bevacizumabbal szemben rezisztensek. Rák . 2010-ben; 116: 5383-5390.
26. Motzer RJ, Michaelson MD, Redman BG, et al. A vaszkuláris endotheliális növekedési faktor receptor és a vérlemezkéből származó növekedési faktor receptor multitestekeredetű inhibitorának SU11248 aktivitása metasztatikus vesesejtes karcinóma esetén. J Clin Oncol. 2006; 24: 16-24.
27. Motzer RJ, Rini BI, Bukowski RM, et al. A Sunitinib metasztatikus vesesejtes karcinóma esetén. JAMA. 2006; 295: 2516-2524.
28. Yang JC, Haworth L, Sherry RM, et al. A bevacizumab, az anti-érrendszeri endothelium növekedési faktor ellenanyag randomizált vizsgálata metasztatikus vesebetegségre. N Engl J Med. 2003; 349: 427-434.
29. Srinivasan R, Su D, Stamatakis L, et al. Mechanizmus alapú célzott terápia örökletes leiomyomatosis és vese sejtrák (HLRCC) és sporadikus papilláris vese-sejt karcinóma: bevacizumab és erlotinib 2. fázisú vizsgálatának közbenső eredményei [absztrakt]. Eur J Cancer. 2014-ig; 50: 8
30. Voss MH, Molina AM, Chen YB és mtsai. II. Fázisú vizsgálat és az everolimusz és a bevacizumab korrelatív genomi analízise a fejlett, nem egyértelmű sejtvese-karcinómában. J Clin Oncol. 2016; 34: 3846-3853.
31. Atkins MB, Hidalgo M, Stadler WM, et al. Fokozatos II. Fázisú vizsgálat a CAC-779 többszörös dózisszintjével, a rapamicin kináz inhibitor új emlős célpontjával, a fejlett refrakter vesesejtes karcinóma esetén. J Clin Oncol. 2004; 22: 909-918.
32. Hutson TE, Escudier B, Esteban E. et al. Temsirolimus vs Sorafenib mint második vonal terápia a metasztatikus vese sejt karcinóma során: az INTORSECT vizsgálat eredményei [absztrakt]. Ann Oncol. 2012; 23: Absztrakt: LBA22.
33. Gordon MS, Hussey M, Nagle RB és mtsai. Az erlotinib II. Fázisú vizsgálata lokálisan előrehaladott vagy metasztatikus papilláris szövettani vese-sejtes rákos betegeknél: SWOG S0317. J Clin Oncol. 2009-ben; 27: 5788-5793.
Ismeretlen elsődleges kezelésű karcinóma (PDQ®) -Patient verzió
Általános tudnivalók az ismeretlen primer karcinómáról
Főbb pontok
- Ismeretlen primer karcinóma (CUP) egy ritka betegség, amelyben rosszindulatú (rákos) sejtek találhatók a szervezetben, de a hely, ahol a rák elkezdődött, nem ismert.
- Néha az elsődleges rákot soha nem találják meg.
- A CUP jelei és tünetei különbözőek, attól függően, hogy a rák a szervezetben terjedt-e.
- Különböző vizsgálatokat alkalmaznak a rák kimutatására.
- Ha a tesztek azt mutatják, hogy rák lehet, akkor biopszia történik.
- Ha a rákos sejtek vagy az eltávolított szövetek típusa eltér a rákos sejtek típusától, várhatóan megtalálható a CUP diagnózisa.
- Az elsődleges rák megtalálásához használt tesztek és eljárások attól függnek, hogy a rák milyen mértékben terjedt el.
- Bizonyos tényezők befolyásolják a prognózist (a helyreállítás esélye).
Ismeretlen primer karcinóma (CUP) egy ritka betegség, amelyben rosszindulatú (rákos) sejtek találhatók a szervezetben, de a hely, ahol a rák elkezdődött, nem ismert.
A szervezet bármilyen szövetében rák képződhet. Az elsődleges daganat (az először kialakult rák) terjedhet a test más részeire. Ezt a folyamatot metasztázisnak nevezik. A rákos sejtek általában olyan sejtekhez hasonlítanak, amelyekben a rák elkezdődött. Például emlőráksejtek terjedhetnek a tüdőbe. Mivel a rák az emlőben kezdődött, a rákos sejtek a tüdőben úgy néznek ki, mint a mellrákos sejtek.
Néha az orvosok megtalálják a rák terjedését, de nem találják meg, hol a szervezetben először nő a rák. Ezt a rákot ismeretlen primer (CUP) vagy okkult primer tumor ráknak nevezik. Nagyít 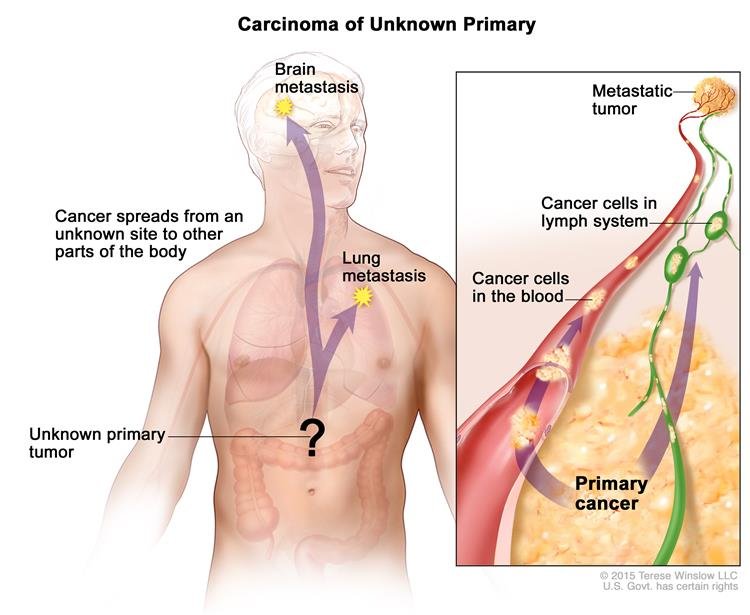
Vizsgálatokat végeznek, hogy megtalálják az elsődleges daganatos megbetegedéseket, és információt kapjanak arról, hogy hol terjed a rák. Amikor a vizsgálatok képesek megtalálni az elsődleges rákot, a rák már nem CUP és a kezelés az elsődleges rák típusán alapul.
Néha az elsődleges rákot soha nem találják meg.
Az elsődleges daganat (az először kialakult rák) nem található az alábbi okok valamelyike miatt:
- Az elsődleges rák nagyon kicsi és lassan növekszik.
- A szervezet immunrendszere megölte az elsődleges rákot.
- Az elsődleges rákot a műtét során eltávolították egy másik állapot miatt, és az orvosok nem tudták, hogy a rák kialakult. Például egy rákos méh eltávolítható egy hysterectomiában a súlyos fertőzés kezelésére.
A CUP jelei és tünetei különbözőek, attól függően, hogy a rák a szervezetben terjedt-e.
Néha a CUP nem okoz semmilyen jelet vagy tünetet. A jeleket és tüneteket a CUP vagy más körülmények okozhatják. Vegye fel a kapcsolatot orvosával, ha rendelkezik az alábbiak bármelyikével:
- A test bármely részében csomósodik vagy megvastagodik.
- Olyan fájdalom, ami a test egy részében van, és nem megy el.
- A köhögés, amely nem megy el, vagy a rekedtség a hangban.
- A bél- vagy húgyhólyag-szokások megváltozása, például székrekedés, hasmenés vagy gyakori vizelés.
- Szokatlan vérzés vagy ürülés.
- Láz nem ismert okból, ami nem megy el.
- Éjjeli izzadás.
- Súlyvesztés nem ismert ok vagy étvágytalanság miatt.
Különböző vizsgálatokat alkalmaznak a rák kimutatására.
A következő tesztek és eljárások alkalmazhatók:
- Fizikai vizsga és történelem: Test a szervezet általános egészségi jeleit ellenőrizni, beleértve a betegség tüneteinek ellenőrzését, például csomókat vagy bármi mást, ami szokatlannak tűnik. A páciens egészségi szokásainak és múltbeli betegségeinek és kezeléseinek története is meg fog történni.
- vizeletvizsgálat: Vizsgálat a vizelet és annak tartalmának, például cukor, fehérje, vér és baktériumok színének ellenőrzésére.
- Vérkémiai vizsgálatok: Olyan eljárás, amely során vérmintát ellenőrizünk a szervezetbe szervek és szövetek vérben felszabaduló egyes anyagok mennyiségének mérésére. Egy szokatlan (magasabb vagy alacsonyabb, mint normál) mennyiségű anyag lehet a betegség jele.
- Teljes vérkép: Olyan eljárás, amely során vérmintát rajzolnak és ellenőrzik az alábbiak szerint:
- A vörösvértestek, a fehérvérsejtek és a vérlemezkék száma.
- A hemoglobin mennyisége (az oxigént hordozó fehérje) a vörösvérsejtekben.
- A minta vörösvérsejtekből álló része.
Ha a tesztek azt mutatják, hogy rák lehet, akkor biopszia történik.
A biopszia a sejtek vagy szövetek eltávolítása, így egy patológus mikroszkóppal nézhető meg. A patológus mikroszkóp alatt vizsgálja a szövetet, hogy keresse meg a rákos sejteket, és megtudja a rák típusát. Az elvégzett biopszia típusa attól függ, hogy a testnek milyen része van a rákban. Az alábbi típusú biopsziák egyike használható:
- Excisziós biopszia: A teljes szövetdarab eltávolítása.
- Szúró biopszia: Egy darab egy részének eltávolítása vagy egy szövetminta eltávolítása.
- Mag biopszia: Szövet eltávolítása széles tűvel.
- Fine-needle aspiration (FNA) biopszia: A vékony tű segítségével eltávolítja a szövetet vagy a folyadékot.
Ha rákot találnak, a következő laboratóriumi tesztek közül egy vagy több alkalmazható a szövetminták tanulmányozására és a rák típusának megállapítására:
- Hisztológiai tanulmány: Olyan laboratóriumi vizsgálat, amelyben a foltokat rákos sejtek vagy szövetek mintájához adják, és mikroszkóp alatt nézve bizonyos változásokat keresnek a sejtekben. A sejtek bizonyos változásai bizonyos rákbetegségekhez kapcsolódnak.
- Immunohisztokémia: Olyan teszt, amely antitesteket használ fel bizonyos antigének ellenőrzésére egy szövetmintában. Az antitest rendszerint radioaktív anyaghoz vagy festékhez kapcsolódik, amely a szövetet mikroszkóp alatt világítja meg. Ezt a fajta vizsgálatot használhatjuk arra, hogy megkülönböztessük a különböző típusú rákok közötti különbséget.
- Fordított transzkripciós polimeráz láncreakció (RT-PCR) teszt: Laboratóriumi vizsgálat, amelyben a szövetmintában lévő sejteket vegyi anyagokkal vizsgálják, hogy bizonyos változásokat keresjenek a génekben.
- Citogenetikai analízis: Laboratóriumi vizsgálat, amelyben a szövetmintában lévő sejteket mikroszkóp alatt vizsgálják, hogy bizonyos változásokat keresjenek a kromoszómákban. Az egyes kromoszómákban bekövetkezett változások egyes rákos megbetegedésekhez kapcsolódnak.
- Fény- és elektronmikroszkópia: Laboratóriumi vizsgálat, amelyben a szövetmintában lévő sejteket rendszeres és nagy teljesítményű mikroszkópokon vizsgálják, hogy bizonyos változásokat keresjenek a sejtekben.
Ha a rákos sejtek vagy az eltávolított szövetek típusa eltér a rákos sejtek típusától, várhatóan megtalálható a CUP diagnózisa.
A test sejtjeinek bizonyos megjelenése függ a szövet típusától. Például a mellrákból vett rákszövet mintája várhatóan mellsejtekből áll. Ha azonban a szövetminta egy másik típusú sejt (amely nem a mellsejtekből áll), akkor valószínű, hogy a sejtek a test másik részétől a mellre terjednek. A kezelés megtervezéséhez az orvosok először megpróbálják megtalálni az elsődleges rákot (az először kialakult rákot).
Az elsődleges rák megtalálásához használt tesztek és eljárások attól függnek, hogy a rák milyen mértékben terjedt el.
Bizonyos esetekben a szervezet azon része, ahol rákos sejteket találnak először, segít az orvosnak eldönteni, mely diagnosztikai tesztek lesznek a leghasznosabbak.
- Ha a daganatot (a légzőszervi betegség alatt lévő vékonyizmokat) a daganat fölött találják meg, az elsődleges daganatos hely valószínűleg a test felső részében, például a tüdőben vagy a mellben található.
- Ha a rák a membrán alatt található, az elsődleges rákhely valószínűleg a test alsó részében, például a hasnyálmirigyben, a májban vagy más szervben van a hasban.
- Egyes rákok általában elterjedtek a test egyes területein. A nyaki nyirokcsomókban található rák esetében az elsődleges daganatos betegség valószínűleg a fejben vagy a nyakában van, mivel a fej- és nyakrák gyakran terjednek a nyirokcsomókban.
A következő vizsgálatokat és eljárásokat lehet elvégezni annak megállapításához, hogy a rák először kezdődött:
- CT vizsgálat (CAT scan): Olyan eljárás, amely a test belsejében lévő területek – például a mellkas vagy a has – részleteit ábrázolja, különböző szögekből. A képeket egy röntgenkészülékhez csatlakoztatott számítógép készítette. A festéket be lehet fecskendezni a vénába, vagy lenyelni, hogy segítsen a szervek vagy szövetek világosabb megjelenítésében. Ezt az eljárást számítógépes tomográfia, számítógépes tomográfia vagy számítógépes axiális tomográfia néven is nevezik.
- MRI (mágneses rezonancia képalkotás): Olyan eljárás, amely egy mágnest, rádióhullámot és egy számítógépet használ a sorozat belsejében lévő részletesebb képek készítéséhez. Ezt az eljárást nukleáris mágneses rezonancia képalkotásnak is nevezik (NMRI).
- PET-vizsgálat (pozitron emissziós tomográfia vizsgálat): Eljárás rosszindulatú sejtek felkutatására a szervezetben. Kis mennyiségű radioaktív glükózt (cukrot) injektálnak a vénába. A PET-szkenner forog a test körül, és képet ad arról, hogy hol van a glükóz. A rosszindulatú daganatsejtek fényesebbek a képen, mert aktívabbak és több glükózzal vesznek fel, mint a normál sejtek.
- mammogram: A mellröntgen.
- Endoszkópia: A szervek és a szövetek belső testének vizsgálatára szolgáló eljárás a rendellenes területek ellenőrzésére. Az endoszkópot a bőrben vagy a testben lévő nyíláson (pl. Az endoszkóp egy vékony, csőszerű eszköz, fényt és lencsét a megtekintéshez. Lehet, hogy van egy eszköze a szövet- vagy nyirokcsomó-minták eltávolítására, amelyeket mikroszkóp alatt ellenőrzik a betegség jelei miatt. Például egy kolonoszkópiát lehet tenni.
- Tumor marker teszt: Olyan eljárás, amely során vér, vizelet vagy szövet mintáját ellenőrizzük bizonyos szervek, szövetek vagy tumorsejtek által a testben előállított bizonyos anyagok mennyiségének mérésére. Bizonyos anyagok bizonyos rákbetegségekhez kapcsolódnak, ha a szervezetben megnövekedett szintek találhatók. Ezeket tumor markereknek nevezik. A vér ellenőrizhető a CA-125, a CgA, az alfa-fetoprotein (AFP), a béta-humán korionos gonadotropin (β-hCG) vagy a prosztata-specifikus antigén (PSA) szintjein.
Néha egyik teszt sem találja az elsődleges rákos helyet. Ezekben az esetekben a kezelés alapja lehet, hogy az orvos úgy gondolja, hogy a legvalószínűbb típusú rák.
Bizonyos tényezők befolyásolják a prognózist (a helyreállítás esélye).
A prognózis (a helyreállítás esélye) a következőktől függ:
- Ahol a rák elkezdődött a testben és ahol terjedt.
- A rákos szervek száma bennük.
- A daganatsejtek mikroszkóp alatt nézve.
- Függetlenül attól, hogy a beteg férfi vagy nő.
- Függetlenül attól, hogy a rákot diagnosztizálták-e vagy visszatérített-e (visszatér).
A legtöbb CUP-ben szenvedő beteg esetében a jelenlegi kezelések nem gyógyítják a rákot. A betegek részt vehetnek a kezelés javítására irányuló számos klinikai vizsgálat egyikében. A CUP klinikai vizsgálatai az ország számos részén zajlanak. A klinikai vizsgálatokkal kapcsolatos információk az NCI honlapján találhatók.
Az ismeretlen primer karcinóma szakaszai
Főbb pontok
- Az ismeretlen primer karcinóma (CUP) nem áll rendelkezésre.
- A rákról ismert információkat a kezelés megtervezésére használják.
Az ismeretlen primer karcinóma (CUP) nem áll rendelkezésre.
A rák terjedelmét vagy terjedését általában szakaszoknak nevezik. A rák állapotát általában a kezelés megtervezésére használják. Azonban a CUP már elterjedt a test más részein, amikor megtalálta.
A rákról ismert információkat a kezelés megtervezésére használják.
Az orvosok az alábbi típusú információkat használják a kezelés megtervezéséhez:
- A szervezetben található hely, ahol megtalálható a rák, például a peritoneum vagy a nyaki (nyak), hónalj (hónalj) vagy inguinális (orgyvér) nyirokcsomók.
- A rákos sejt típusa, például a melanoma.
- Függetlenül attól, hogy a ráksejt rosszul differenciált (a mikroszkóp alatt nézve nagyon eltér a normál sejtektől).
- A rákos megbetegedések és tünetek.
- A vizsgálatok és eljárások eredményei.
- Függetlenül attól, hogy a rák újonnan diagnosztizált vagy újból felbukkan-e (visszatér).
Kezelési opció áttekintése
Főbb pontok
- Az ismeretlen primer karcinómában (CUP) szenvedő betegek különböző típusú kezelést alkalmaznak.
- Négyféle standard kezelést használnak:
- Sebészet
- Sugárkezelés
- kemoterápiás kezelés
- Hormonterápia
- A klinikai vizsgálatok során új típusú kezelést tesztelnek.
- A betegek esetleg gondolkodni akarnak a klinikai vizsgálatban való részvételről.
- A betegek klinikai vizsgálatokat végezhetnek rákkezelésük előtt, alatt vagy után.
Az ismeretlen primer karcinómában (CUP) szenvedő betegek különböző típusú kezelést alkalmaznak.
Különböző típusú kezelések állnak rendelkezésre a CUP-ben szenvedő betegek számára. Néhány kezelés standard (jelenleg alkalmazott kezelés), és néhányat klinikai vizsgálatokban tesztelnek. A kezelés klinikai vizsgálata egy olyan kutatási tanulmány, melynek célja a jelenlegi kezelések javítása vagy a rákos betegek új kezeléseivel kapcsolatos információk beszerzése. Amikor a klinikai vizsgálatok azt mutatják, hogy az új kezelés jobb, mint a hagyományos kezelés, az új kezelés válhat a szokásos kezelésnek. A betegek esetleg gondolkodni akarnak a klinikai vizsgálatban való részvételről. Néhány klinikai vizsgálat csak olyan betegek számára nyitott, akik nem kezdték meg a kezelést.
Négyféle standard kezelést használnak:
A műtét a CUP közös kezelése. Az orvos eltávolíthatja a rákot és néhány egészséges szövetet körülötte.
Miután az orvos eltávolít minden rákot, amely a műtét idején látható, egyes betegek kemoterápiát vagy sugárterápiát kaphatnak a műtét után, hogy megöljék a rákos sejteket. A műtét után adott kezelést, hogy csökkentse a rák visszaszorulásának kockázatát, az adjuváns terápiának nevezik.
Sugárkezelés
A sugárterápia olyan rákkezelés, amely nagy energiájú röntgenfelvételt vagy egyéb sugárzást használ fel a rákos sejtek megölése vagy növekedésük megakadályozására. Kétféle sugárkezelés létezik:
- A külső sugárterápia a testen kívüli gépet sugárzásnak sugározza a rák felé. A sugárkezelés bizonyos módjai segítenek megakadályozni a sugárzást a közeli egészséges szövetek károsításában. Ez a sugárterápiás kezelés magában foglalhatja a következőket:
- Intenzitás modulált sugárterápia (IMRT): Az IMRT egy háromdimenziós (3-D) sugárterápiás módszer, amely számítógépet használ a daganat méretének és alakjának képalkotására. A különböző intenzitású sugárzók vékony sugarai (erősségei) sokféle szögre irányulnak a tumorra. Ez a fajta külső sugárterápia kevésbé károsítja a közeli egészséges szöveteket, és kevésbé valószínű, hogy szájszárazságot, nyelési nehézséget és a bőr károsodását okozza.
A sugárkezelés módja attól függ, hogy milyen típusú rákot alkalmaznak. A külső és belső sugárterápiát ismeretlen primer karcinóma kezelésére alkalmazzák.
kemoterápiás kezelés
A kemoterápia egy olyan rákkezelés, amely a rákos sejtek növekedését megakadályozó gyógyszereket használ, akár a sejtek megölésével, akár megakadályozva azok elosztását. Ha a kemoterápiát szájon át vagy vénába vagy izomba injektálják, a gyógyszerek bejutnak a véráramba, és rákos sejteket érhetnek el a szervezetben (szisztémás kemoterápia). Ha a kemoterápiát közvetlenül a cerebrospinális folyadékba, egy szervbe vagy egy testüregbe, például a hasba helyezik, a gyógyszerek elsősorban a rákos sejteket érintik ezen a területen (regionális kemoterápia). A kombinált kemoterápia két vagy több rákellenes gyógyszer alkalmazása.
Hormonterápia
A hormonterápia olyan rákkezelés, amely eltávolítja a hormonokat, vagy blokkolja működését, és megakadályozza a rákos sejtek növekedését. A hormonok olyan anyagok, amelyeket a mirigyek a szervezetben termelnek és a véráramban keringenek. Egyes hormonok bizonyos rákos megbetegedéseket okozhatnak. Ha a vizsgálatok azt mutatják, hogy a rákos sejtek olyan helyeket tartalmaznak, ahol a hormonok kötődhetnek (receptorok), gyógyszerek, műtét vagy sugárterápia alkalmazható a hormontermelés csökkentésére vagy a működés megakadályozására.
A klinikai vizsgálatok során új típusú kezelést tesztelnek.
A klinikai vizsgálatokkal kapcsolatos információk az NCI honlapján találhatók.
A betegek esetleg gondolkodni akarnak a klinikai vizsgálatban való részvételről.
Néhány beteg esetében a klinikai vizsgálatban való részvétel lehet a legjobb kezelés választása. A klinikai vizsgálatok része a rákkutatási folyamatnak. Klinikai kísérleteket végeztünk annak megállapítására, hogy az új rákkezelések biztonságosak és hatékonyak-e vagy jobbak-e, mint a szokásos kezelés.
A mai rák elleni szokásos kezelések közül sok a korábbi klinikai vizsgálatokon alapul. A klinikai vizsgálatban részt vevő betegek a szokásos kezelést kapják, vagy az elsők között új kezelést kaphatnak.
A klinikai vizsgálatokban részt vevő betegek segítenek a jövőben a rák kezelésének javításában is. Még akkor is, ha a klinikai vizsgálatok nem eredményeznek hatékony új kezeléseket, gyakran válaszolnak fontos kérdésekre és elősegítik a kutatás továbbterjedését.
A betegek klinikai vizsgálatokat végezhetnek rákkezelésük előtt, alatt vagy után.
Néhány klinikai vizsgálatban csak olyan betegek tartoznak, akik még nem részesültek kezelésben. Az egyéb kísérletek vizsgálati kezelése olyan betegeknél, akiknek a rákja nem javult. Vannak klinikai vizsgálatok is, amelyek új módszereket próbálnak megakadályozni a rák előfordulásának visszatéréséből (visszatérés) vagy a rák kezelésének mellékhatásainak csökkentésében.
Klinikai vizsgálatok zajlanak az ország számos részén. Az NCI által támogatott klinikai vizsgálatokkal kapcsolatos információk megtalálhatók az NCI klinikai vizsgálata weboldalán. Más szervezetek által támogatott klinikai vizsgálatok megtalálhatók a ClinicalTrials.gov weboldalon.
Az ismeretlen primer karcinóma kezelési lehetőségei
Az újonnan diagnosztizált ismeretlen primer karcinóma
Nyaki nyaki nyirokcsomók
A cervicalis (nyaki) nyirokcsomókban található rák terjedhet a fej vagy a nyak daganatából. Az ismeretlen primer (CUP) nyaki nyirokcsomók karcinóma kezelése a következőket foglalhatja magában:
- Sebészet eltávolítása a mandulák.
- Csak sugárkezelés. Intenzitás modulált sugárterápiát (IMRT) alkalmazhatunk.
- Radiációs terápia, amelyet műtét követ a nyirokcsomók eltávolítására.
- Operáció a nyirokcsomók eltávolítására, sugárkezeléssel vagy anélkül.
- Az új típusú kezelések klinikai vizsgálata.
Rosszul differenciált karcinómák
A rosszul differenciált ráksejtek nagyon különböznek a normál sejtektől. A sejt típusát nem ismerjük. Az ismeretlen primer, rosszindulatúan differenciált karcinóma, beleértve a daganatokat a neuroendokrin rendszerben (az agy azon része, amely hormontermelő mirigyeit szabályozza egész testen) tartalmazhatja a következőket:
- Kombinációs kemoterápia.
- Az új típusú kezelések klinikai vizsgálata.
Peritoneális rákban szenvedő nők
Az olyan nők esetében, akiknél a peritoneális (a hasüreg bélése) ismeretlen primer karcinóma megegyezik a petefészekrákkal. A kezelés a következőket foglalhatja magában:
- Kemoterápia.
- Az új típusú kezelések klinikai vizsgálata.
Elszigetelt axilláris nyirokcsomó metasztázis
A csak a hónalj (hónalj) nyirokcsomóiban található rák terjedhet a mellrákban.
A hónalj nyirokcsomó metasztázis kezelése általában:
- Műtét eltávolítása a nyirokcsomókban.
A kezelés magában foglalhatja a következők közül egyet vagy többet is:
- Műtét eltávolítása a mell.
- Sugárterápia a mellre.
- Kemoterápia.
- Az új típusú kezelések klinikai vizsgálata.
Inguinalis nyirokcsomó metasztázis
A rák csak a lágyéki nyirokcsomókban (gennyes, anális, rektális) kezdett. A lymphoma nyirokcsomó metasztázis kezelése a következőket foglalhatja magában:
- Műtét a rák és / vagy a nyirokcsomók eltávolítása az ágyékban.
- Operáció a rák és / vagy a nyirokcsomók eltávolítására az ágyékban, majd sugárterápia vagy kemoterápia.
Melanoma egy egységes nyirokcsomó területen
A melanoma kezelésére, amely csak egy nyirokcsomó területen található, általában:
- Műtét eltávolítása a nyirokcsomókban.
Lásd a PDQ összegzést a melanoma kezelésről további információkért.
Többszörös részvétel
Az ismeretlen primer karcinómában nincs egységes kezelés, amely a test különböző területein található. A kezelés a következőket foglalhatja magában:
- Hormonterápia.
- Belső sugárterápia.
- Egy vagy több rákellenes gyógyszerrel végzett kemoterápia.
- Egy klinikai vizsgálat.
Az ismeretlen primer ismétlődő karcinóma
Az ismeretlen primer ismétlődő karcinóma kezelése általában egy klinikai vizsgálaton alapul. A kezelés a következőktől függ:
- A rák típusát.
- Hogyan kezelték a rákot.
- Ahol a rák visszatért a szervezetbe.
- A beteg állapota és kívánságai.
A klinikai vizsgálati keresés segítségével megtaláljuk az NCI által támogatott rákos klinikai vizsgálatokat, amelyek elfogadják a betegeket. A rák típusától, a páciens korától és a kísérletek elvégzésétől függően vizsgálatokat végezhet. A klinikai vizsgálatokkal kapcsolatos általános információk is rendelkezésre állnak.
A klinikai vizsgálati keresés segítségével megtaláljuk az NCI által támogatott rákos klinikai vizsgálatokat, amelyek elfogadják a betegeket. A rák típusától, a páciens korától és a kísérletek elvégzésétől függően vizsgálatokat végezhet. A klinikai vizsgálatokkal kapcsolatos általános információk is rendelkezésre állnak.
Tudjon meg többet az ismeretlen primer karcinómáról
Az Országos Rákkutató Intézet további, az ismeretlen primer rákos megbetegedésekkel kapcsolatos további információkért lásd:
Az Országos Rákkutató Intézet általános rákos információira és egyéb erőforrásaira vonatkozóan lásd:
Erről a PDQ-összefoglalóról
Az orvos adatkérdése (PDQ) az Országos Rákkutató Intézet (NCI) átfogó rákinformációs adatbázisa. A PDQ adatbázis tartalmazza a rák megelőzésére, kimutatására, genetikájára, kezelésére, támogató gondozására és kiegészítő és alternatív gyógymódokra vonatkozó legfrissebb információk összefoglalóit. A legtöbb összefoglaló két változatban jelenik meg. Az egészségügyi szakemberek részletes leírása technikai nyelven íródott. A páciens verziója könnyen érthető, nem technikai nyelven készült. Mindkét verzió rákos információkkal rendelkezik, pontos és naprakész, és a legtöbb változat spanyolul is elérhető.
A PDQ az NCI szolgáltatása. Az NCI az Országos Egészségügyi Intézetek (NIH) része. A NIH a szövetségi kormány biomedikai kutatásának központja. A PDQ-összefoglalók az orvosi szakirodalom független felülvizsgálatán alapulnak. Ezek nem az NCI vagy az NIH politikai nyilatkozatai.
Ennek az összefoglalónak a célja
Ez a PDQ rákinformáció összefoglalása aktuális információt tartalmaz az ismeretlen primer karcinóma kezeléséről. Célja, hogy tájékoztassa és segítse a betegeket, családokat és gondozóikat. Nem nyújt hivatalos iránymutatásokat és ajánlásokat az egészségügyi ellátásról szóló döntések meghozatala érdekében.
Felülvizsgálók és frissítések
A szerkesztői testületek írják le a PDQ rákinformációs összefoglalásait, és naprakészen tartják azokat. Ezek a bizottságok rákkezeléssel foglalkozó szakemberek és a rákkal kapcsolatos egyéb specialitásokból állnak. Az összefoglalókat rendszeresen felülvizsgálják, és új információkkal kerülnek módosításra. Az összes összefoglaló dátuma (“Utolsó módosítás dátuma”) a legfrissebb változás dátuma.
A betegtájékoztatóban szereplő információk az egészségügyi szakemberek által készített verzióból származnak, amelyet rendszeresen felülvizsgálnak és szükség szerint frissítenek a PDQ Adult Treatment Editorial Board.
Klinikai kísérleti információk
A klinikai vizsgálat olyan vizsgálat, amely egy tudományos kérdés megválaszolására szolgál, például arról, hogy az egyik kezelés jobb-e a másiknál. A kísérletek a múltbeli vizsgálatokon és a laboratóriumi tapasztalatokon alapulnak. Minden kísérlet megfelel bizonyos tudományos kérdéseknek annak érdekében, hogy új és jobb módszereket találjanak a rákos betegek segítésére. A kezelés során a klinikai vizsgálatok során információt gyűjtenek az új kezelés hatásairól és arról, hogy mennyire jól működik. Ha egy klinikai vizsgálat azt mutatja, hogy az új kezelés jobb, mint a jelenleg alkalmazott, akkor az új kezelés “normál” lesz. A betegek esetleg gondolkodni akarnak a klinikai vizsgálatban való részvételről. Néhány klinikai vizsgálat csak olyan betegek számára nyitott, akik nem kezdték meg a kezelést.
A klinikai vizsgálatok szerepelnek a PDQ-ban, és megtalálhatók az NCI honlapján. Számos rákos orvos is részt vesz a klinikai vizsgálatokban. További információkért hívja az 1-800-4-CANCER rák tájékoztató szolgálatot (1-800-422-6237).
Engedély az összefoglaló használatához
A PDQ bejegyzett védjegy. A PDQ-dokumentumok tartalmát szabadon szövegként lehet használni. Nem azonosítható NCI PDQ rák információs összefoglaló, hacsak az egész összefoglaló nem látható, és rendszeresen frissül. Azonban a felhasználó számára megengedett, hogy írjon egy mondatot, például: “Az NCI PDQ rákról szóló összefoglalója az emlőrák megelőzéséről a következőképpen állapítja meg a kockázatokat: [az összefoglaló kivonatát].”
A PDQ összegzésének legjobb módja a következő:
PDQ® Felnőtt Kezelés Szerkesztőség. Ismeretlen elsődleges kezelés PDQ karcinóma. Bethesda, MD: National Cancer Institute. Frissítve. Elérhető: https://www.cancer.gov/types/unknown-primary/patient/unknown-primary-treatment-pdq. Hozzáférés. [PMID: 26389238]
Az összefoglalóban szereplő képeket a szerző (k), a művész és / vagy a kiadó engedélyével használják a PDQ-összefoglalókban való használatra. Ha PDQ-összefoglalóból szeretne képet használni, és nem használja az egész összefoglalót, akkor a tulajdonosnak engedélyt kell kapnia. A Nemzeti Rákkutató Intézet nem adhatja meg. Az összefoglalóban szereplő képek használatával kapcsolatos információk és a rákkal kapcsolatos számos egyéb kép megtalálható a Visuals Online-ban. A Visuals Online több mint 2000 tudományos kép gyűjteménye.
lemondás
Az összefoglalókban szereplő információk nem használhatók a biztosítási díjakra vonatkozó döntések meghozatalára. A biztosítási fedezetről bővebben a Cancer.gov webhelyen találhatók a kezelői rákkezelési oldalon.
Lépjen kapcsolatba velünk
További információért forduljon hozzánk, vagy segítséget kapjon a Cancer.gov weboldalán a Kapcsolatfelvétel a Súgó oldalon. Kérdések a Cancer.gov weboldalon keresztül is elérhetők.
- Frissítve: 2018. március 23
Az Országos Rákkutató Intézet honlapján található legtöbb szöveg szabadon felhasználható vagy újra használható. A Nemzeti Rákkutató Intézetet forrásnak kell tekinteni, és ehhez az oldalhoz kapcsolódó linket is be kell vonni, például az “Ismeretlen Primer Terápiás Karcinóma (PDQ®) -Patient Version eredetileg a National Cancer Institute kiadta.”
Kérjük, vegye figyelembe, hogy a kormányon kívüli egyének által készített blogbejegyzések tulajdonosa lehet az író tulajdonosa, és a grafika tulajdonosa lehet az alkotója. Ilyen esetekben kapcsolatba kell lépni az íróval, művészekkel vagy kiadóval, hogy engedélyt szerezzen az újrafelhasználásra.
Üdvözöljük a hozzászólásait ezen a bejegyzésen. Az összes megjegyzésnek meg kell felelnie a megjegyzéss politikának.
Szeretné használni ezt a tartalmat webhelyén vagy más digitális platformon? A szindikációs szolgáltatás oldalunk megtudja, hogyan.


Kommentek
Kommenteléshez kérlek, jelentkezz be: